SILEN-Studien: BI 201335 auf dem Prüfstand
Der neue Proteasehemmer BI 201335 von Boehringer Ingelheim wurde in SILEN-1 bei Therapienaiven und in SILEN-2 bei vorbehandelten Patienten in zwei Dosierungen (120mg bzw. 240mg einmal täglich) geprüft. Alle Patienten erhielten 24 Wochen Triple-Therapie gefolgt ggf. von 24 Wochen pegIFN/RBV. Bei zwei Gruppen war zudem eine 3tägige Einleitungsphase mit pegIFN/RBV vorgeschaltet.
Ergebnisse
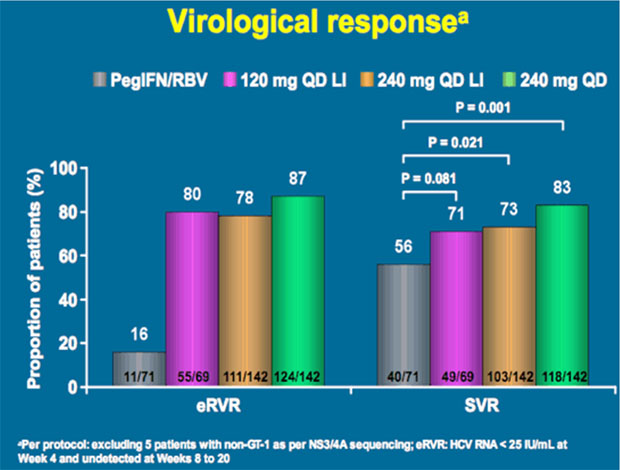
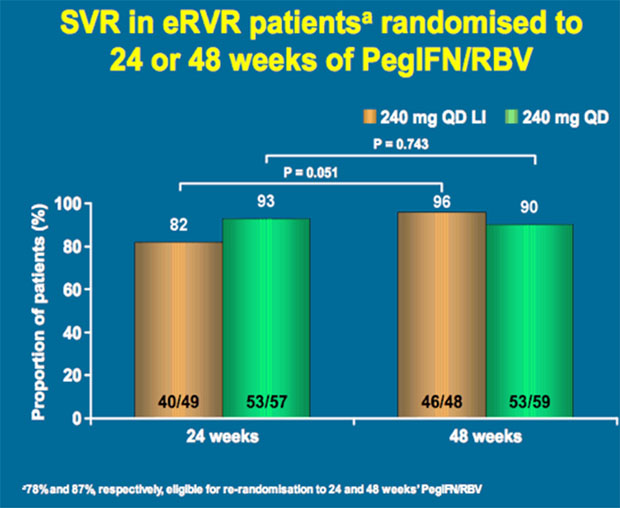
In SILEN-1 erreichten bis zu 83% der Patienten eine SVR, wobei 87% nach RVR die Therapie schon nach 24 Wochen beenden konnten.
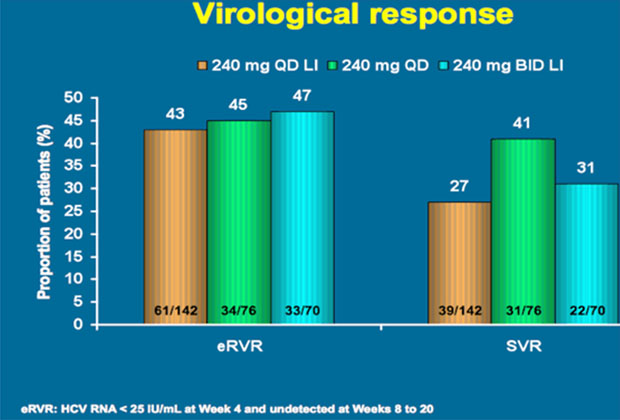
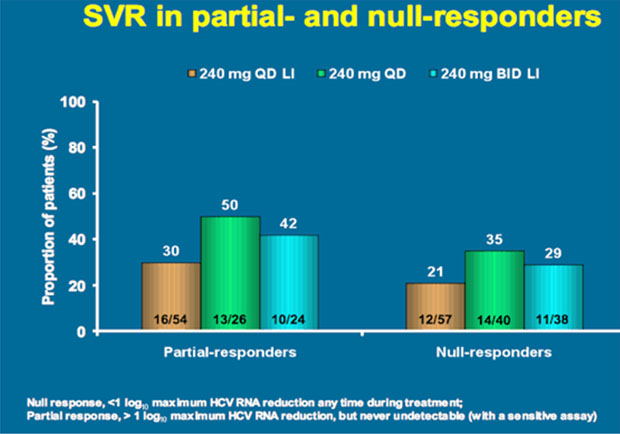
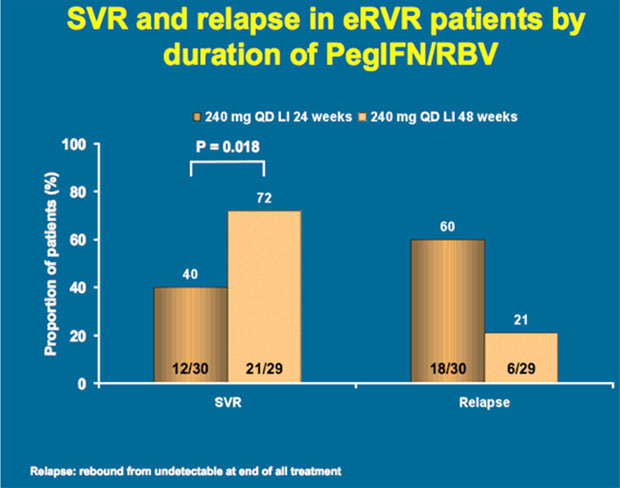
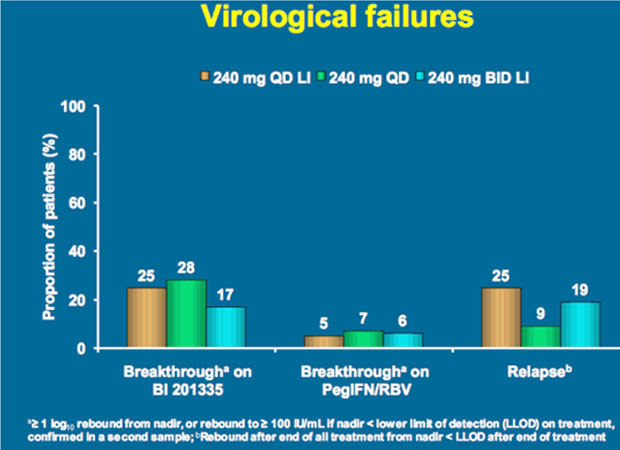
In SILEN-2 erreichten bis zu 41% der vorbehandelten Patienten eine SVR, wobei sich die Therapieverkürzung bei Patienten mit raschem Ansprechen hier als ungünstig erwies.
Die 3tägige Einleitungsphase hatte keinen Effekt.
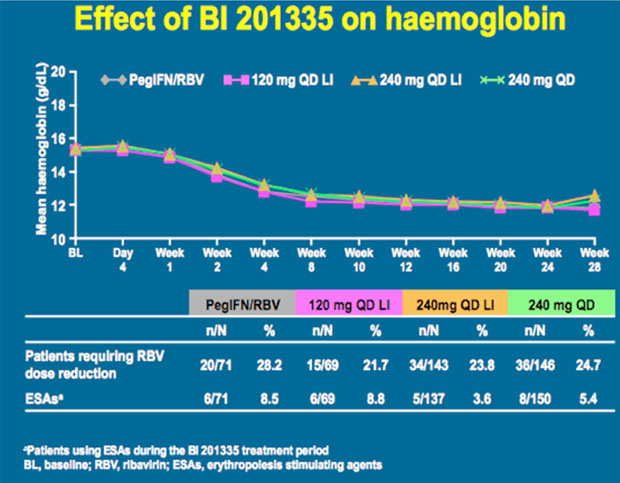
Die Verträglichkeit war im Allgemeinen gut. Häufigste Nebenwirkung war ein leichter Ikterus, der auf eine isolierte indirekte Hyperbilirubinämie zurückgeht.
In den geplanten Phase-3-Studien soll die 240 mg-Dosierung eingesetzt werden.
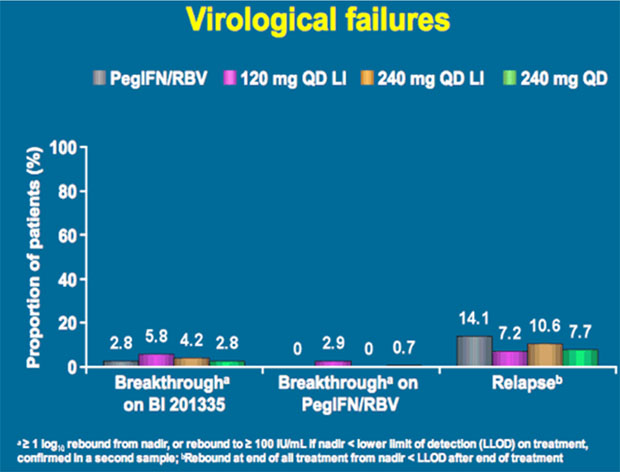
SILEN-1


SILEN-2


SILEN-2
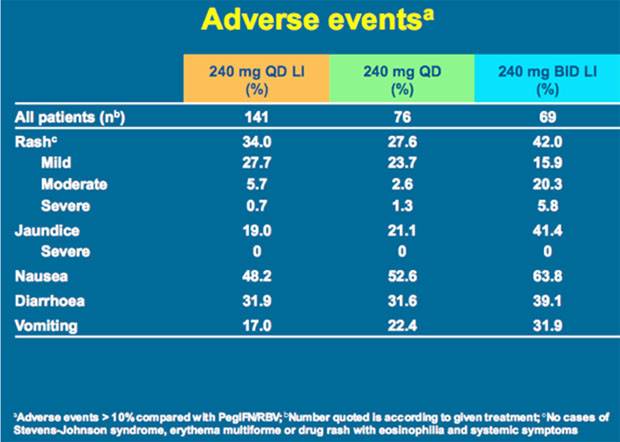
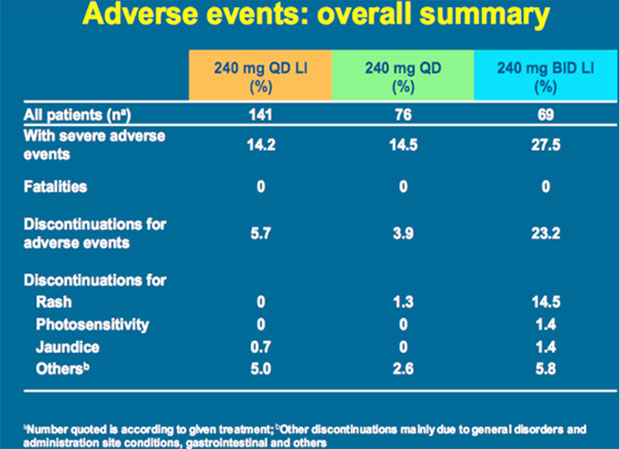
Bilder: www.natap.org





