GECCO-Kohorte: Einfluss von RAS oder RBV auf den Therapieerfolg von Sofosbuvir (SOF)/ Velpatasvir (VEL) bei GT 3-Infektion
Hintergrund und Zielsetzung
Die Kombination aus Sofosbuvir (SOF) und Velpatasvir (VEL) ist seit Juli 2016 in Europa zur Therapie der chronischen Hepatitis C zugelassen. Bis Sommer 2017 stellte diese die Standardtherapie für alle Patienten mit HCV Genotyp 2 und 3 Infektion in Deutschland dar. In der ASTRAL-3-Zulassungsstudie für den HCV Genotyp 3 waren Baseline Resistenzen im NS5A Gen mit einem höheren Relapse-Risiko assoziiert. Auch Genotyp-3-Patienten mit Zirrhose, insbesondere solche, die bereits eine Vortherapie erhalten hatten, wiesen höhere Relapseraten auf. Für beide Patientengruppen wird die Notwendigkeit einer Kombination von SOF/VEL mit Ribavirin zur Verhinderung eines Relapses diskutiert. GECCO ist eine prospektive, multizentrische HCV-Kohorte an 9 Studienzentren in Deutschland, in der alle Patienten, die seit Februar 2014 eine HCV-Therapie erhalten haben, dokumentiert werden. Ziel der vorliegenden Arbeit war es den Einfluss von Baseline NS5A-Resistenzen und Zirrhose auf die Ansprechraten in einer großen Genotyp-3-Real-World-Kohorte zu untersuchen.
Abbildung: SOF/VEL +- RBV für 12 Wochen bei HCV Genotyp 3
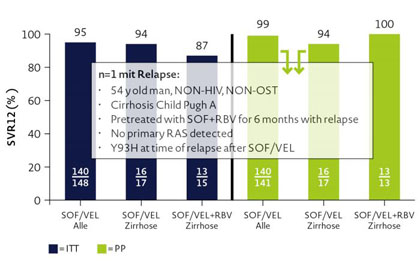
Methodik
Alle Genotyp-3-Patienten der GECCO-Kohorte, die eine SOF/VEL-Therapie mit oder ohne Ribavirin erhalten hatten wurden in der vorliegenden Arbeit analysiert. Besonderes Augenmerk wurde auf den Einfluss von Baseline-Resistenzen, Vortherapie und Zirrhose auf das Therapieansprechen gelegt.
Ergebnisse
In der gesamten GECCO-Kohorte waren zum Analysezeitpunkt 2312 Patienten eingeschlossen. Hiervon waren 576 Patienten mit dem Genotyp 3 infiziert, von denen wiederum 232 Patienten mit SOF/VEL ± Ribavirin behandelt wurden. Insgesamt 14 % (n=32/232) hatten eine Kombinationstherapie mit Ribavirin erhalten. Eine Analyse der Patienten-Charakteristika zu Baseline ergab folgendes Bild: 69 % Männer, medianes Alter 47 Jahre, 11 % waren HIV-koinfiziert. Eine gleichzeitige Opioidsubstitution erhielten 37 % und 22 % wiesen eine Zirrhose auf (90 % mit Child Pugh A-Zirrhose). Schließlich waren 76 % (n=177/232) der Patienten auf Baseline Resistenzen getestet worden. Hiervon wiesen 9 % (n=16/232) eine Resistenz im NS5A-Gen auf. Nur die klinisch relevanten Resistenzenan den NS5A-Positionen A30 und Y93 wurden gewertet. Da einige Patienten noch unter Therapie bzw. im Follow-Up waren, konnten insgesamt 148 bzw. 141 Patienten in der ITT- bzw. PP-Analyse (ohne „lost to follow-up“) ausgewertet werden. Die SVR12-Rate lag bei 95 % (n=140/148) bzw. 99 % (n=140/141). In der gesamten Kohorte fand sich lediglich 1 Patient mit virologischem Therapieversagen. Dieser hatte eine Child Pugh A-Zirrhose und kein Ribavirin erhalten, allerdings war er auch mit SOF+Ribavirin für 24 Wochen vortherapiert. Vor Therapie wies er keine NS5A-Resistenzen auf, nach SOF/VEL-Versagen ließ sich jedoch die Y93H Substitution detektieren. Alle Zirrhose-Patienten, die Ribavirin erhalten hatten wurden geheilt (PP-Analyse). Zirrhose-Patienten mit/ohne Ribavirin unterschieden sich zudem nicht wesentlich bezüglich ihrer Baseline-Charakteristika. Alle Patienten mit Baseline-Resistenzen wurden geheilt.
Fazit
In dieser großen deutschen Real-World-Kohorte konnten die hohe Wirksamkeit der SOF/VEL-Kombination aus dem ASTRAL-Studienprogramm bestätigt werden. Bis auf einen Patienten wurden alle nachbeobachteten Patienten geheilt. Ein additiver Nutzen für Ribavirin bei Patienten mit Zirrhose konnte nicht gezeigt werden. Baseline Resistenzen hatten ebenfalls keinen Einfluss auf das Therapieansprechen.
 PD Dr. med. Johannes Vermehren
PD Dr. med. Johannes Vermehren
Oberarzt der Medizinischen Klinik I,
Universitätsklinikum Frankfurt,
Theodor-Stern-Kai 7,
60590 Frankfurt am Main
Kommentar PD Dr. med. Johannes Vermehren
Die vorliegende Arbeit aus der GECCO-Kohorte greift wichtige Fragen bei der HCV-Therapie von Genotyp-3-Patienten auf: Spielt Ribavirin noch eine Rolle, insbesondere bei zirrhotischen Patienten? Welchen Einfluss haben Baseline-Resistenzen auf das Therapieansprechen? Da VEL/SOF-Patienten initial nicht in das Deutsche Hepatitits-C-Register eingeschlossen werden konnten, stellt die GECCO-Kohorte die einzige größere deutsche Kohorte dar, in der diesen Fragen nachgegangen werden kann. Insbesondere gibt die Studie (bei allerdings kleiner Fallzahl) einen Hinweis, dass bei Child Pugh A-Zirrhose möglicherweise auf die zusätzliche Gabe von Ribavirin verzichtet werden kann. Es sei jedoch angemerkt, dass es sich wie bei allen Real-World-Kohorten nicht um eine randomisierte Studie handelt. Insofern können natürlich vom jeweiligen Behandler instinktiv die etwas kränkeren Patienten mit fortgeschrittenerer Zirrhose mit Ribavirin behandelt worden sein, auch wenn der Vergleich der Baseline-Charakteristika hierfür keinen Hinweis gibt (Patienten mit und ohne Ribavirin unterschieden sich lediglich bezüglich des Baseline-INR). Darüber hinaus wurden kaum Patienten mit dekompensierter Zirrhose (Child B/C) behandelt, die noch am ehesten von Ribavirin profitieren, wie die ASTRAL-4 Studie gezeigt hat (Curry et al. NEJM 2015). Die zweite wichtige Frage ist die nach dem Einfluss von Baseline-Resistenzen. Hier zeigte sich, dass alle Patienten mit Baseline Resistenzen geheilt wurden (n=4/10 hatten RBV erhalten).
 Prof. Dr. med.
Prof. Dr. med.
Wolf-Peter Hofmann
Gastroenterologie am
Bayrischen Platz,
Innsbrucker Str. 58,
D-10825 Berlin
Kommentar Prof Dr. med. Wolf-Peter Hofmann
Patienten mit HCV-Genotyp 3 und kompensierter Zirrhose stellen nach wie vor eine problematische Subgruppe von HCV-Patienten dar. Die Daten der nicht-gesponserten, unabhängigen GECCO-Kohorte zeigt, dass die Kombination aus VEL/SOF über 12 Wochen unabhängig von präexistenten Resistenz-assoziierten Substitutionen (RAS) und unabhängig einer zusätzlichen Gabe von Ribavirin bei dem Genotyp 3 exzellente SVR Raten erzielt. Die erfahrenen Zentren der GECCO-Kohorte hatten bei 15 der 32 GT3-Patienten mit HCV- assoziierter Zirrhose SOF/VEL mit Ribavirin kombiniert. Bei der relativ kleinen Fallzahl kam es zu einem einzigen virologischen Relapse ohne Ribavirin, jedoch hatte der Patient bereits eine Vortherapie mit Sofosbuvir und Ribavirin über 24 Wochen erhalten.





