Kilian Weigand, Regensburg
Genotyp 3 – Update 2015
Nur
wenige der sieben seit Januar 2014 zugelassenen direkt antiviral
wirksamen Substanzen (DAAs – direct acting antivirals) (Sofosbuvir,
Simeprevir, Paritaprevir, Daclatasvir, Ledipasvir, Ombitasvir und
Dasabuvir) weisen eine breite pangenotypische Wirkung auf und haben
daher auch eine gute Wirksamkeit gegen den Genotyp 3 (GT 3). Das
schränkt die Therapieoptionen bei diesem Genotyp relativ ein und
insbesondere bei Patienten mit vorbestehender Leberzirrhose ist die
Datenlage unzureichend. Tabelle 1 aus dem Addendum 2/15 zu der
aktuellen deutschen Empfehlung zur Therapie der chronischen Hepatitis
C (Sarrazin et al (2015)) zeigt einen Überblick über die möglichen
Therapieoptionen des GT 3. Daraus wird ersichtlich, dass es aktuell
nur für die DAAs Sofosbuvir, Daclatasvir und Ledipasvir eine
Zulassung beim GT 3 gibt und für die anderen DAAs beim GT 3 keine
Daten zur Verfügung stehen oder keine effektive Wirksamkeit besteht.
| Therapieregime | Dauer (Wo.) | Pat. ohne Zirrhose | Pat. mit komp. Zirrhose | ||
|---|---|---|---|---|---|
| TN 1 | TE 2 | TN 1 | TE 2 | ||
| SOF + RBV | 24 | x | x | x 4 | (x) 3,4 |
| SOF + DCV | 12 | x | x | |
|
| SOF + LDV + RBV | 12 | (x) 3 | (x) 3 | |
|
| SOF + DCV + RBV | 24 | x 4 | |||
| SOF + LDV + RBV | 24 | (x) 3,4 | |||
| 1TN, therapienaiv; 2 TE, therapieerfahren; (i.d.R. Vorbehandlung mit (PEG)-Interferon +/- RBV) 3 Diese Therapie ist nur mit Einschränkungen zu empfehlen (siehe Erläuterungen) 4 Alternativ kann bei entsprechender Verträglichkeit auch eine Triple-Therapie mit SOF, PEG-Interferon und RBV durchgeführt werden. | |||||
Tabelle 1:Übersicht über die Therapieoptionen beim Genotyp 3. Tabelle aus dem Addendum zur Hepatitis C Leitlinie 2/15 mit den aktuellen Empfehlungen zur Therapie der chronischen Hepatitis C (Sarrazin et al. 2/15 im Auftrag der Fachgesellschaften).
SOF = Sofosbuvir; RBV = Ribavirin; DCV = Daclatasvir; LDV = Ledipasvir
Sofosbuvir
Bei Sofosbuvir (SOF) handelt es sich um einen nukleosidischen NS5B-Polymeraseinhibitor. Dieses DAA weist eine starke pangenotypische Wirksamkeit und daher eine gute Aktivität gegen den GT 3 auf. SOF hat zudem eine sehr hohe Resistenzbarriere. Es wird als 400 mg Tablette einmal täglich verabreicht. Da es renal ausgeschieden wird und keinen CYP3A/4 Metabolismus aufweist, sind wenige Medikamenteninteraktionen zu erwarten. Allerdings wurden in den letzten Monaten einige schwere Bradykardien in Kombination mit dem Antiarrhythmikum Amiodaron beschrieben, weswegen ein aktueller Rote-Hand-Brief vor der gemeinsamen Verwendung warnt. Amiodaron sollte daher vor einer antiviralen Therapie abgesetzt oder umgestellt werden.
Leider
war die Effektivität von Sofosbuvir in Kombination mit Ribavirin
(RBV) beim GT 3 und einer Therapiedauer von 12 Wochen sehr gering. So
ergab die initiale Studie (FISSION) nur eine SVR-Rate von 61 %
bei Patienten ohne Zirrhose und von nur 34 %
bei Patienten mit Zirrhose. Erst die Verlängerung der Therapie auf
24 Wochen wie in der Nachfolge-
Studie (VALENCE) untersucht,
führte bei therapienaiven Patienten zu einer SVR-Rate von 95 %
bzw. 92 %
bei Patienten ohne bzw. mit Leberzirrhose. Bei therapieerfahrenen
Patienten lag die SVR-Rate allerdings nur bei 87 %
ohne und 62 %
mit Leberzirrhose. Ergänzend muss hier aufgeführt werden, dass in
den Studien die Patientenzahlen sehr gering waren, insbesondere in
den Subgruppen mit Leberzirrhose.
In einer sehr kleinen Studie mit insgesamt 24 Patienten (LONESTAR-2) wurde die Therapie mit SOF und RBV über 12 Wochen zusätzlich mit pegyliertem Interferon ergänzt. Hier zeigte sich eine SVR-Rate von 83 % unabhängig davon, ob eine Leberzirrhose vorlag oder nicht. Daher könnte der GT 3 mit kompensierter Leberzirrhose eine letzte Domäne für Interferon darstellen. Dies sollte jedoch eine Einzelfallentscheidung bleiben und generell gilt auch beim GT 3, dass eine interferonhaltige Therapie nicht mehr empfohlen ist.
In den genannten Studien gab es sehr wenige schwerwiegende Nebenwirkungen. Zusammengefasst kann daher die Therapie mit SOF und RBV als gut verträgliche und sichere Therapie angesehen werden. Allerdings ist eine Therapiedauer von 24 Wochen notwendig und damit bei Patienten ohne Leberzirrhose gegenüber einer anderen Therapie (auch im Hinblick auf Dauer und Kosten) ungünstiger (s.u.). Nur bei therapienaiven Patienten mit kompensierter Leberzirrhose ist diese Therapie eine sinnvolle Alternative.
Daclatasvir
Für den GT 3 stellt die Kombination aus SOF mit dem NS5A-Inhibitor Daclatasvir (DAC) sicherlich derzeit die effektivste Therapie dar. DAC weist beim GT 3 in vitro eine fast ebenso gute antivirale Effektivität wie beim GT 1 auf. Es wird als 60 mg Tablette einmal täglich verabreicht und weist aufgrund seines Stoffwechselweges ebenfalls nur sehr wenige Medikamenteninteraktionen auf. In der initialen Zulassungsstudie von DAC (Sulkowski et al (2014) N Engl J Med) wurden 18 therapienaive Patienten mit DAC, SOF und RBV über 24 Wochen behandelt. Davon erreichten 89 % eine SVR, unabhängig von der Gabe von RBV – bei dieser allerdings sehr kleinen Patientenzahl. Umso erstaunlicher, wenngleich sehr erfreulich, war eigentlich die initiale Zulassung von DAC auch für GT 3 Patienten.
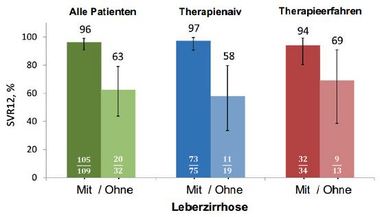
Abbildung 1:ALLY-3 Studie (Nelson et al (2015) Hepatology). SVR-Raten nach einer Therapie von therapienaiven oder therapieerfahrenen GT 3 Patienten mit oder ohne Leberzirrhose über 12 Wochen mit Daclatasvir (DAC) 60 mg/d und Sofosbuvir (SOF) 400 mg/d.
Die entscheidenden Daten lieferte die Studie ALLY-3 (Nelson et al (2015) Hepatology). Hier wurden 101 therapienaive und 51 therapieerfahrene (keine Vortherapie mit einem NS5A-Inhibitor) Patienten über 12 Wochen mit der Kombination aus DAC und SOF therapiert. RBV wurde nicht hinzugegeben. Eine Leberzirrhose wiesen ca. 20 % der therapienaiven und ca. 25 % der vorbehandelten Patienten auf. Die Abbildung 1 fasst die wichtigsten Ergebnisse zusammen. Bei Patienten ohne Leberzirrhose zeigte sich eine sehr hohe SVR-Rate von 97 % bei therapienaiven und 94 % bei therapieerfahrenen Patienten. Daher stellt bei Patienten mit einer GT 3 Infektion ohne Zirrhose die 12-wöchige Kombination aus DAC und SOF die effektivste und sinnvollste Therapie dar. Bei Patienten mit Zirrhose jedoch fielen die SVR-Raten deutlich ab auf 58 % bzw. 69 % ohne bzw. mit Vortherapie. Hier ist zu bemerken, dass in beiden Armen nur bei sehr wenigen Patienten eine Leberzirrhose vorlag. In weiteren Subgruppenanalysen war insbesondere ein fortgeschrittenes Alter ein Prädiktor für ein schlechteres Ansprechen. Wie zu erwarten war die Verträglichkeit der Therapie sehr gut. Fast alle Therapieversager erlitten einen Relaps, während das Ansprechen auf die Therapie initial gut war.
Ergänzend kann man hier die von Hezode et al auf der EASL 2015 präsentierten Daten betrachten. Dieser stellte Daten aus dem französischen Compassionate Use Program zu Patienten mit einer GT 3 Infektion vor. Insgesamt wurden die Daten von 601 Patienten gezeigt. Damit handelt es sich um die bislang größte präsentierte Real Life Datensammlung zu GT 3 Patienten. Alle diese Patienten wurden mit der Kombination aus DAC und SOF behandelt. Nur bei etwa 20 % wurde ergänzend Ribavirin hinzugegeben. Insgesamt waren jeweils 75 % der Patienten männlich, vortherapiert und hatten eine F4-Fibrose. Die SVR-Raten lagen hier bei Patienten ohne Leberzirrhose bei 92 % bei einer 12-wöchigen und bei 83 % bei einer 24-wöchigen Therapiedauer. Mit Leberzirrhose lagen die SVR-Raten bei 76 % (12 Wochen) bzw. 88 % (24 Wochen).
Zusammengefasst liegt damit die SVR-Rate bei therapienaiven Patienten mit kompensierter Leberzirrhose nicht wesentlich höher als bei der Kombination aus SOF und RBV alleine und kann daher nicht unbedingt primär empfohlen werden. Bei vorbehandelten Patienten mit kompensierter Leberzirrhose stellt die Kombination aus DAC und SOF über 24 Wochen jedoch die derzeit effektivste Therapieoption dar. Der Stellenwert von RBV ist in dieser Kombination noch nicht letztlich geklärt, könnte aber, insbesondere bei GT 3 Patienten mit Leberzirrhose, einen optionalen Zusatznutzen bringen.
Ledipasvir
Der zweite zugelassene NS5A-Inhibitor Ledipasvir (LDV) ist als 90/400 mg Kombinationstablette mit SOF koformuliert zugelassen. Auch dieses Präparat wird einmal täglich eingenommen, weist ein geringes Medikamenteninteraktionspotential auf und ist sehr gut verträglich. Zwar besteht eine Zulassung für den GT 3, allerdings ist die Effektivität von LDV beim GT 3 um etwa den Faktor 1000 geringer als gegenüber dem GT 1. Es zeigte sich in der ersten Studie zum GT 3 (ELECTRON-2) mit insgesamt 51 Patienten daher auch nur eine SVR-Rate von 64 % bei therapienaiven Patienten ohne Leberzirrhose bei einer 12-wöchigen Therapiedauer. Durch die ergänzende Gabe von RBV konnte die SVR-Rate auf 100 % gesteigert werden. Eine weitere sehr kleine Studie (n=28) wies nach einer 12-wöchigen Therapie von therapieerfahrenen GT 3 Patienten mit SOF/LDV und RBV eine SVR-Rate von 89 % ohne und von 73 % mit Leberzirrhose auf (Gane et al (2014) Hepatology). Die Kombination aus SOF/LDV und RBV kann daher bei einzelnen GT 3 Patienten eine Therapieoption darstellen, sollte aber nicht generell als primäre Therapieoption in Betracht gezogen werden.
HIV-koinfizierte Patienten
Zwar gibt es nur wenige Daten, die sich gezielt mit GT 3 Patienten und einer HIV-Koinfektion auseinandersetzten, aber die generelle Datenlage zur HCV/HIV-koinfizierten Patienten zeigt klar auf, dass diese Population nicht anders zu behandeln ist als HCV-Monoinfizierte. Dies war auch beim GT 3 nicht anders zu erwarten und wurde auf der EASL 2015 durch die Daten der ALLY-2 Studie bestätigt, in der sich bei Koinfizierten mit GT 3 unter einer Therapie mit DAC und SOF vergleichbare SVR-Raten wie bei den Monoinfizierten fanden. Hinzu kommt, dass die für den GT 3 zugelassenen DAAs ein sehr geringes Interaktionspotential zu den antiretroviralen Substanzen aufweisen.
Zukunftsperspektive
Insgesamt besteht derzeit bei Patienten mit GT 3 durchaus eine gute Therapieoption mit den zugelassenen DAAs. Allerdings sind die Therapieoptionen wesentlich eingeschränkter als zum Beispiel beim GT 1 und die Datenlage in einzelnen Subgruppen beruht oft auf sehr wenigen Patienten. Hier können jedoch bald weitere Real Life Daten erwartet werden, insbesondere aus dem Deutschen Hepatitis C-Register.
Problematisch ist sicherlich auch die Frage wie mit Therapieversagern auf die primäre Therapie umzugehen ist. Hierzu gibt es bislang keine Empfehlungen und die Tatsache, dass beide beim GT 3 wirksamen Substanzklassen dann bereits eingesetzt worden sind, macht diese Frage noch schwieriger. Ob dies eine (letzte) Domäne für pegyliertes Interferon werden wird, ist allerdings zweifelhaft, insbesondere angesichts der eingeschränkten Verwendbarkeit von Interferon bei Patienten mit Leberzirrhose.
Viel Neues beim GT 3 wird allerdings nicht so rasch zu erwarten sein. Das wurde auch auf der EASL 2015 deutlich. Von den zuletzt noch sehr interessanten Substanzen Alisporivir (Inhibitor der Interaktion von Cyclophilin A) und BIT225 (Blocker des p7-Protein von HCV), die beide auch gegen GT 3 aktiv waren, wurden keine neuen Daten präsentiert. Gezeigt wurden experimentelle Studien mit RG-101, einem Inhibitor der micro-RNA122, der auch eine Potenz gegen GT 3 aufwies. Ob sich hieraus jedoch eine therapeutische Option ergeben wird, bleibt abzuwarten.
Deutlich weiter in der Entwicklung ist der pangenotypisch-wirksame NS5A-Inhibitor GS-5816, eine deutliche stärkere Effektivität gegen den GT 3 aufweist als LDV. Allerdings würden in Koformulierung mit SOF letztlich nur die beiden bereits bekannten Substanzklassen zum Einsatz kommen mit oder ohne RBV. Ebenfalls aus dieser Substanzklasse wurden initiale Daten zu dem pangenotypischen nukleosidischen Polymeraseinhibitor MK-3682 präsentiert.
Ein Lichtblick
Ein Lichtblick war die C-SWIFT Studie. Hier wurden therapienaive GT 3 Patienten mit und ohne Leberzirrhose über 8 bzw. 12 Wochen mit einer Kombination aus SOF und Grazoprevir/Elbasvir behandelt. Es fand sich eine hohe SVR-Rate bei diesen Patienten. Somit steht mit Grazoprevir vielleicht bald erstmals ein NS3/4A Protease-Inhibitor zur Therapie des GT 3 zur Verfügung. Ebenfalls in Entwicklung befindlich ist der pangenotypische NS3/4A Protease-Inhibitor GS-9857. Diese Protease-Inhibitoren könnten für Patienten mit einem Therapieversagen auf eine der aktuell zugelassenen Regime eine gute Therapieoption darstellen.





