Ramona Pauli, München
Neue Leitlinien Tripletherapie der Hepatitis C
Der Prozess zur Leitlinienerstellung ist standardisiert und Erstellung von S3-Leitlinien mit der höchsten Wertigkeit ist sehr aufwändig und zeitintensiv. Aus diesem Grund entschloss man sich, die bisherige S3-Leitlinien zur Hepatitis C nicht zu aktualisieren, sondern eine S1-Leitlinie zu verfassen, die formal eine Expertenmeinung darstellt.
HCV-Monoinfektion
Die Empfehlungen zur Therapie der HCV-Monoinfektion mit Genotyp 1 wurde von einem kleinen Expertengremium erstellt,
jedoch waren alle Autoren auch an den S3-Leitlinien beteiligt. Die Experten sprechen sich bei therapie-
naiven
Patienten für eine primäre Tripletherapie aus, wobei bei Patienten mit günstigen Voraussetzungen für ein rasches
virologisches Ansprechen auf pegyliertes Interferon und Ribavirin (d.h. keine fortgeschrittene Fibrose, HCV-RNA <
600.000-800.000 IU/ml, günstiger IL28B-Genotyp) auch eine Standardtherapie erwogen werden kann.
Bei vorbehandelten Patienten ist eine Tripletherapie indiziert. Je besser die Patienten auf die Vortherapie angesprochen haben, umso höher sind die Chancen auf eine Heilung unter Tripletherapie. Bei Patienten mit Leberzirrhose und Null-response in der Vortherapie liegen die Heilungschancen bei Telaprevir <15 %. Bei Boceprevir waren die SVR-Raten in einer Interimanalyse einer kleinen Studie ähnlich niedrig.
Die Indikationsstellung zur antiviralen Therapie bei besonderen Patientengruppen wie Patienten mit Begleiterkrankungen, Suchterkrankungen, Organtransplantationen usw. hat sich nicht grundlegend geändert. Bei diesen Patientengruppen liegen allerdings noch keine ausreichenden Erfahrungen vor. Einschränkungen ergeben sich insbesondere durch Medikamentenwechselwirkungen.
Prädiktoren
Die bekannten Prädiktoren für eine Heilung (z.B. Viruslast, IL28B-Genotyp, Fibrosegrad, LDL-Cholesterin, Ansprechen auf Vortherapie) sind zwar auch bei der Tripletherapie Prädiktoren für das Ansprechen auf Interferon, ihr Stellenwert ist jedoch aufgrund der hohen direkt antiviralen Wirksamkeit der HCV-Proteasehemmer geringer. Neu ist, dass Subtyp 1a mit einer höheren Resistenz- und niedrigeren Heilungsrate assoziiert ist. 92% aller viralen Durchbrüche traten bei HCV-Subtyp-1a auf. Wichtiges prog-nostisches Kriterium ist das Ansprechen zu Woche 4.
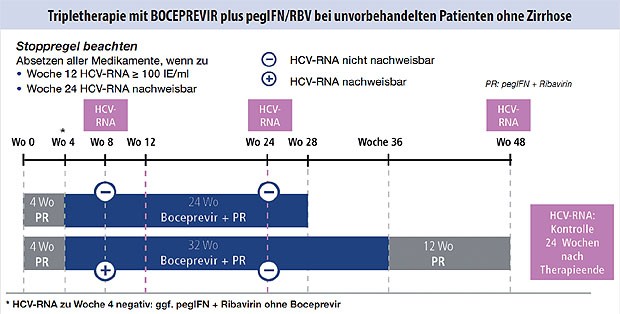
Abbildung 1: Unvorbehandelte Patienten ohne Zirrhose
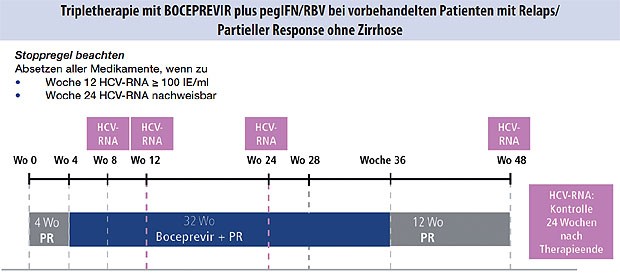
Abbildung 2: Partielle Response oder Relapse in der
Vortherapie, keine Zirrhose

Abbildung 3: Null-Response in der Vortherapie und Patienten mit Zirrhose
Algorithmen
Es gibt für die Erst- und Retherapie mit Boceprevir (Abb. 1-3) und Telaprevir (Abb. 4 und 5) besondere Algorithmen.
Ein vierwöchiges Lead in mit pegyliertem Interferon und Ribavirin ermöglicht die individuelle Evaluation der
Suszepibilität gegenüber der dualen Kombinationstherapie. Dies könnte insbesondere von Nutzen sein bei unvorbehandelten
Patienten, wenn bei RVR der Verzicht auf eine Tripletherapie zur Diskussion steht sowie bei Patienten mit
fortgeschrittener Fibrose/Zirrhose und Nullresponse in der Vortherapie, denn bei einem Abfall der HCV-RNA beim Lead in
von <1 log bedeutet eine SVR-Chance von nur ca. 10 %.
Stopp-Regeln
Eine Fortführung der Gabe des Protease-inhibitors bei fehlendem virologischen Ansprechen führt zunehmend zur Selektion von Resistenzen mit hoher Replikationseffektivität und möglicherweise langer Persistenz und sollte daher unbedingt vermieden werden. Nicht zuletzt ist ein möglichst frühzeitiges Erkennen eines Therapieversagens auch kosteneffizient. In der Analyse erreichte kein einziger Patient mit einer HCV-RNA-Viruslast >1.000 IU/ml zu Woche 4 unter Telaprevir trotz Fortsetzung der Kombinationstherapie eine SVR. Auch für Boceprevir fand sich eine 100 % negative Prädiktion für eine fehlende SVR bei einer Viruslast >100 IU/ml zu Woche 12 (Woche 8 der Tripletherapie). Zwischen Boceprevir und Telaprevir besteht eine komplette Kreuzresistenz.
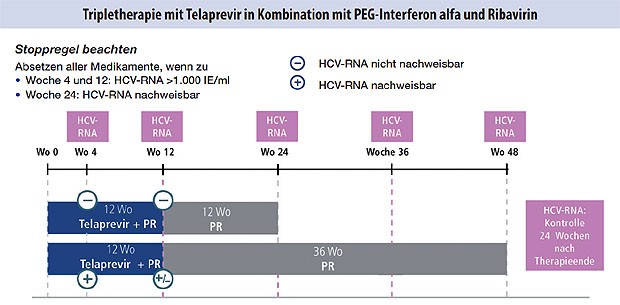
Abbildung 4: Unvorbehandelte Patienten und Patienten mit
Relapse, keine Zirrhose
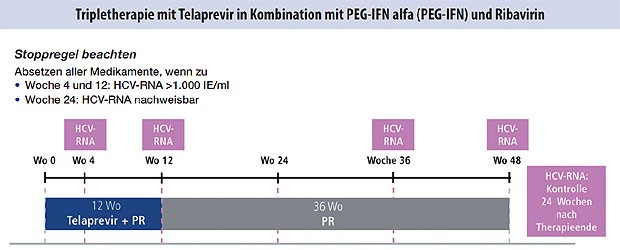
Abbildung 5: Partielle Response und Null-Response in der
Vortherapie, alle Patienten mit Zirrhose
Wechselwirkungen
Es gibt zahlreiche Wechselwirkungen mit den Boceprevir und Telaprevir, die teils klassen-, teils substanzspezifisch sind. Hier wird die Beachtung der Fachinformation sowie die Konsultation aktueller Daten empfohlen und als Datenbank www.hep-druginteractions.org genannt.
Nebenwirkungen
Das Nebenwirkungsmanagement ist entscheidend für den Therapieerfolg. Zu den Nebenwirkungen von pegyliertem Interferon und Ribavirin kommen noch die Nebenwirkungen der HCV-Proteasehemmer hinzu. Eine Dosisreduktion ist bei den Proteasehemmern nicht möglich. Häufigste Nebenwirkungen von Tela-previr sind der Hautausschlag, die Verstärkung der Anämie und gastrointestinale Beschwerden. Bei Boceprevir sind es die Verstärkung der Anämie und eine Geschmacksstörung.
Die Leitlinien stehen zur Verfügung bei www.deutsche-leberstiftung.de.
HCV/HIV-Koinfektion
Die Leitlinien zur HCV/HIV-Koinfektion wurden von Jürgen Rockstroh, Bonn, Patrick Ingiliz, Berlin, und Axel
Baumgarten, Berlin, verfasst und stellen ebenfalls S1-Leitlinien, d.h. Expertenmeinungen dar. Das Management der
Patienten richtet sich nach dem HCV-
Therapiestatus und dem Fibrosegrad der Leber bzw. der Fibroseprogression.
Indikation
Bei Patienten mit F4-Fibrose sollte man in jedem Fall mit den derzeit verfügbaren Proteasehemmern eine Triple-
therapie versuchen, wobei Patienten mit Leberzirrhose in spezialisierten Zentren behandelt werden sollten. Ebenso sollte
man HCV-therapienaiven Patienten und Relapser mit einer signifikanten Fibrose (F2/F3) jetzt mit Tripletherapie
behandeln, denn eine schwere Fibrose/Zirrhose vermindert die Heilungschancen nach bisherigem Wissen auch bei den
zukünftigen Therapieoptionen.
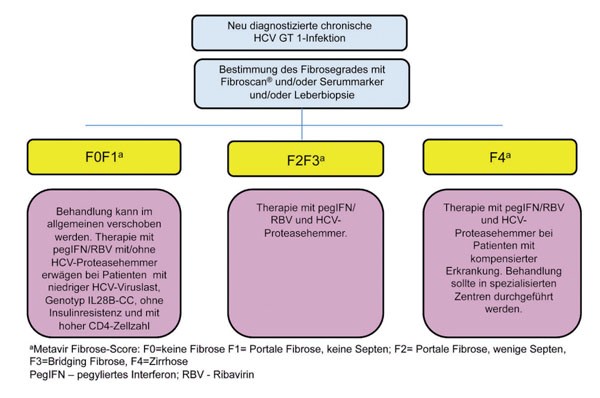
Abbildung 6: Management der neu diagnostizierten HIV/HCV Koinfektion Genotyp
1. Nach Ingiliz P, Rockstroh J Liver International 2012, in press
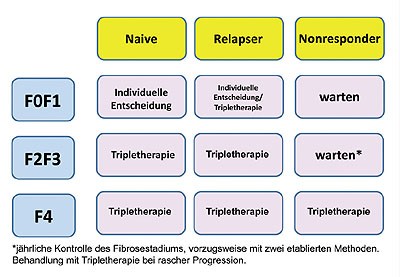
Abbildung 7: Therapie der HIV/HCV-Koinfektion Genotyp 1 gemäß Fibrosegrad und Ansprechen
auf vorherige Therapie. Nach Ingiliz P, Rockstroh J Liver International 2012, in press
Lediglich bei HCV-Nonrespondern ohne Zirrhose (F0-F3) kann/sollte man auf neue Optionen warten, die besser verträglich, einfacher und möglicherweise auch noch wirksamer sind.
In diesen Fällen wird jedoch eine regelmäßige Kontrolle des Fibrosegrades empfohlen, um bei rascher Progression doch
noch vor Entwicklung einer F4-Fibrose die Tripletherapie einzuleiten (Abb. 6 und 7).
Wechselwirkungen
Grundsätzlich können beide HCV-Proteasehemmer bei der HIV/HCV-Koinfektion eingesetzt werden. Dabei ist bei
Koinfizierten als Besonderheit das unterschiedliche Wechselwirkungsprofil von Boceprevir und Telaprevir mit
antiretroviralen Substanzen zu beachten (Abb. 8 und 9).
Wie schon in der Standardtherapie, sollte der Nukleosidbackbone zur Vermeidung von Toxizitäten aus ABC/3TC oder TDF/FTC bzw. 3TC bestehen.
| HiV-Medikament | Empfehlung |
|---|---|
| Studien abgeschlossen | |
| Atazanavir/r | Im Allgemeinen nicht empfohlen. EMEA: Kann individuell erwogen werden, wenn keine Resistenzen vorliegen und Viruslast supprimiert ist |
| darunavir/r Fosamprenavir/r lopinavir/r | Nicht empfohlen |
| Efavirenz | Nicht empfohlen |
| raltegravir | Keine Dosisanpassung notwendig |
Abbildung 8: Wechselwirkungen von Boceprevir mit antiretroviralen Medikamenten
| HiV-Medikament | Empfehlung |
|---|---|
| Studien abgeschlossen | |
| Atazanavir/r | Klinische und Laborkontrollen der Hyperbilirubinämie empfohlen |
| darunavir/r Fosamprenavir/r lopinavir/r | Nicht empfohlen |
| Efavirenz | Erhöhung der Telaprevir-Dosis (1.125 mg q8h) |
| raltegravir | Keine Dosisanpassung notwendig |
| tenofovir | Vermehrte klinische und Laborkontrollen notwendig |
Abbildung 9: Wechselwirkungen von Telaprevir mit antiretroviralen Medikamenten
Die Wechselwirkung mit anderen Medikamenten z.B. Statinen, Antihyperten-siva, usw. ist auch bei HIV-Infizierten zu beachten. Zu beachten ist ferner, dass die Wechselwirkungen von HCV-Proteasehemmer und ART plus andere Medikamente, die am CYP 450 Cytochrom verstoffwechselt werden, nicht untersucht und schwer kalkulierbar sind. Erhöhte klinische Aufmerksamkeit sowie gegebenenfalls Spiegelmessung der antiretro-viralen Substanzen können hier im Einzelfall weiterhelfen.





