Arndt Weinmann, Marcus A. Wörns, Peter R. Galle, Mainz
Sorafenib bei fortgeschrittenem HCC
Molekulare Hepatokarzinogenese
Die molekularen Hepatokarzinogenese ist von einer hohen Komplexität geprägt, jedoch werden bestimmte Signalwege als besonders relevant für die Entstehung und Progression des HCC angesehen. Neben intrazellulären Signalwegen wie dem MAP-Kinase Signalweg bestehend aus den zentralen Komponenten Ras/Raf/MEK/ERK werden die Rezeptortyrosinkinasen bestimmter Wachstums- und Angiogenesefaktoren wie VEGF (vascular endothelial growth factor), PDGF (platelet derived growth factor) oder EGF (epidermal growth factor) als ideale Ziele dieser zielgerichteten Therapie (targeted therapy) angesehen. Im Zentrum des klinischen Interesses stehen daher vor allem Substanzen, die über diese Angriffspunkte in die Proliferation und Neoangiogenese des HCC eingreifen können.
Das Hepatozelluläre Karzinom (HCC) ist weltweit der sechsthäufigste Tumor und die dritthäufigste tumorassoziierte Todesursache. Das Vorliegen einer Leberzirrhose stellt per se den wichtigsten Risikofaktor für die Entstehung eines HCC dar, wobei das Risiko in Abhängigkeit von der zugrunde liegenden Lebererkrankung variiert. Das HCC hat aufgrund des endemischen Auftretens der Hepatitis B Virus (HBV) Infektion eine hohe Prävalenz in Asien und Afrika. In Japan und den westlichen Industrienationen steigt die Inzidenz aufgrund der Verbreitung der Hepatitis C Virusinfektion in den letzten Jahren kontinuierlich an. Darüber hinaus spielen ätiologisch die nutritiv-toxische Leberzirrhose sowie die Zunahme der nichtalkoholischen Steatohepatitis (NASH) eine entscheidende Rolle.
Nur jeder 3. kurativ behandelbar
Der häufig zur Klassifikation des HCC genutzte Barcelona Liver Cancer Clinic (BCLC)-Score gibt über seine algorithmische Komponente Auskunft über die anzustrebende Therapie in Abhängigkeit von Tumorstadium, Leberfunktion und Allgemeinzustand (Abb. 1). Da der Tumor häufig erst in einem späten Stadium diagnostiziert wird, steht lediglich für ca. 30% der Patienten bei Erstdiagnose ein potentiell kuratives Verfahren (Resektion, Lebertransplantation, Radiofrequenzablation) zur Verfügung. Palliative Therapiekonzepte wie die transarterielle Chemoembolisation (TACE) kommen für Patienten mit multifokalem Tumorwachstum in Frage, wobei sich ein Überlebensvorteil nur bei asymptomatischen Patienten mit gut erhaltener Leberfunktion und fehlender Pfortaderthrombose gezeigt hat. Bei Patienten mit lokal weit fortgeschrittener Tumorerkrankung mit Gefäßinfiltration und insbesondere beim Vorliegen einer extrahepatischen Manifestation hat keine der in den letzten Jahren im Rahmen einer systemischen Chemotherapie eingesetzten Substanzen – alleine oder als Kombinationstherapie – höhere Ansprechraten als 25% bzw. einen Überlebensvorteil bei nicht zu unterschätzendem Nebenwirkungsprofil gezeigt. Dies liegt einerseits an der ausgeprägten Resistenz des HCC gegenüber zytotoxischen Substanzen, wie sie z.B. über das multidrug resistance protein (MDR1) vermittelt wird, und zum anderen an der im Regelfall zugrunde liegenden Leberzirrhose, die ihrerseits mit einer erhöhten Mortalität verbunden ist und aufgrund der eingeschränkten hepatischen Reserve die Aggressivität der Therapie limitiert.
Trotz häufigem Einsatz von Substanzen wie Doxorubicin oder Cisplatin muss festgestellt werden, dass es bis vor kurzem keine etablierte Standardtherapie des fortgeschrittenen HCC gab. Ein besseres Verständnis der molekularen Hepatokarzinogenese hat in den letzten Jahren jedoch neue Therapieansätze ermöglicht.
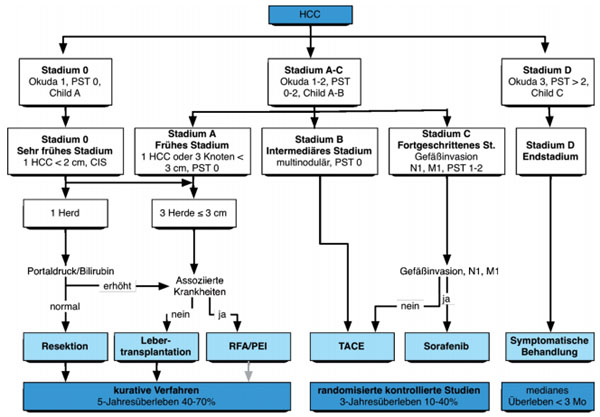
Abb. 1: Der BCLC Score1
Der Multikinase-Inhibitor Sorafenib
Sorafenib ist ein oraler Multikinase-Inhibitor, der neben intrazellulären Kinasen (Raf-1/B-Raf) verschiedene Rezeptortyrosinkinasen inhibiert, wobei insbesondere die Hemmung von VEGFR-2/-3 und PDGFR-ß von entscheidender Bedeutung sind. Damit werden sowohl Signalwege im Tumor mit dem Ergebnis einer gesteigerten Apoptose als auch in der genetisch stabilen Endothelzelle blockiert.
Im Rahmen einer Phase-II-Studie mit 137 Patienten konnte durch den Einsatz von Sorafenib das ermutigende Ergebnis eines medianen Gesamtüberlebens von 9,2 Monaten bei fortgeschrittenem HCC erreicht werden.
Die SHARP-Studie
Im Jahr 2007 wurden die Ergebnisse der SHARP-Studie (Sorafenib HCC
Assessment Randomized Protocol Trial) im New England Journal of Medicine
publiziert.2 Die Studie untersuchte den Einsatz von Sorafenib bei
Patienten mit fortgeschrittenem HCC. Um einen Konfounder-Effekt der
zugrundeliegenden Leberzirrhose auszuschließen, sahen die Einschlusskriterien
eine Limitierung auf Patienten mit Leberzirrhose im Stadium Child-Pugh A vor.
Insgesamt wurden 602 Patienten in die Studie
eingeschlossen, davon 299 in der Verumgruppe. Primärer Endpunkt war das
Gesamtüberleben. Es zeigte sich eine signifikante Verbesserung des medianen
Überlebens um 2,8 Monate (10,7 Monate mit Sorafenib vs. 7,9 Monate mit Placebo,
p=0,0077, HR 0,69). Auch die Zeit bis zur Tumorprogression hatte sich fast
verdoppelt (5,5 Monate mit Sorafenib vs. 2,8 Monate mit Placebo). Durch diese
Studie konnte erstmals eine Verbesserung des Gesamtüberlebens bei einer
systemischen Therapie des HCC demonstriert werden. Aufgrund der Daten wurde
Sorafenib von der FDA und der EMEA Ende 2007 für die Therapie des HCC
zugelassen.
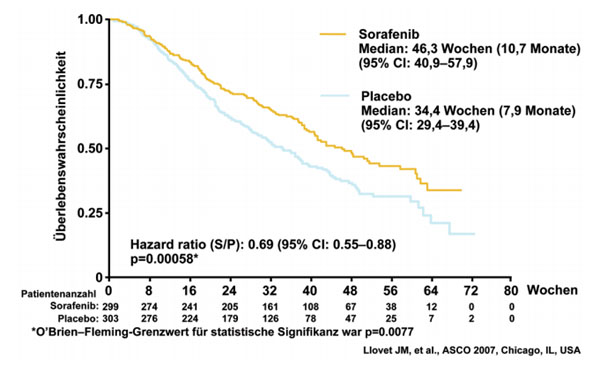
Abb. 2: Kaplan-Meier-Kurve des Gesamtüberlebens in
der SHARP-Studie2
Nebenwirkungen der Sorafenib-Therapie
Insgesamt waren Therapie-assoziierte Nebenwirkungen in der SHARP-Studie häufig, die Rate über alle Schweregrade betrug 80% in der Sorafenib-Gruppe versus 52% in der Placebo-Gruppe. Die meisten Nebenwirkungen waren jedoch vom Schweregrad 1 oder 2 und waren mit symptomatischer Behandlung zu bewältigen. Bei den Grad 3 Nebenwirkungen dominierten Diarrhoen (8%), das Hand-Fuß-Syndrom (8%), eine arterielle Hypertonie sowie abdominelle Schmerzen (2%). Aufgrund von Nebenwirkungen musste bei 26% eine Dosisreduktion bzw. bei 44% eine Behandlungsunterbrechung durchgeführt werden, letztendlich musste jedoch bei lediglich 10% der Patienten die Therapie aufgrund von Nebenwirkungen beendet werden.
Therapie bei fortgeschrittener Leberzirrhose
Im Rahmen der SHARP-Studie wurde das verbesserte Gesamtüberleben durch die Sorafenib-Therapie nur bei Patienten mit Leberzirrhose im Stadium Child-Pugh (CP) A nachgewiesen. Die Zulassung der Substanz enthält dagegen keine Einschränkung in Bezug auf die Leberfunktion.
In der Mehrzahl der Fälle haben HCC-Patienten mit einer extrahepatischen Manifestation auch eine fortgeschrittene Leberzirrhose. Im klinischen Alltag stellt sich damit die Frage, ob eine Sorafenibtherapie auch bei diesen Patienten einen Benefit bringt.
Daten bei Child-Pugh B
Einige Studien mit kleinen Patientenzahlen haben diese Frage untersucht. Von Abou-Alfa wurden 2008 auf der Tagung der American Society of Clinical Oncology die Ergebnisse der CP-B-Patienten aus der Phase-II-Studie von Sorafenib vorgestellt.3 Die beobachteten Toxizitäten der 38 Patienten waren bei Fatigue, Hand-Fuß-Syndrom und Diarrhoe vergleichbar mit denen der CP-A-Patienten. Im Gegensatz dazu waren leberassoziierte Nebenwirkungen wie Hyperbilirubinämie, Encephalopathie und Aszites deutlich häufiger, wobei eine Abgrenzung zwischen einer Therapienebenwirkung und einer Verschlechterung der Leberfunktion nicht eindeutig möglich war. Therapieunterbrechungen oder Dosismodifikationen waren bei CP-B-Patienten nicht häufiger notwendig als bei CP-A-Patienten. Es konnte nur eine deutlich kürzere Therapiedauer der CP-B-Patienten von 12,9 Wochen im Vergleich zur CP-A-Gruppe mit 24,9 Wochen erreicht werden. Auch die Überlebenszeit der CP-B-Patienten war mit 3,3 Monaten gegenüber 9,4 Monaten deutlich reduziert.
Weitere Studien
In einer Studie aus Mainz wurden insgesamt 34 Patienten retrospektiv analysiert. 15 Patienten wiesen keine Zirrhose oder eine Leberzirrhose im Stadium CP A, 15 Patienten ein Stadium CP B und 4 Patienten ein Stadium CP C auf. Wie bei Abou-Alfa zeigten sich deutlich mehr Leberdysfunktionen in der Gruppe der CP B und CP C-Patienten und es fanden sich erneut deutliche Unterschiede im Überleben mit 7,2 Monate bei CP A, beziehungsweise 3,3 und 3,4 Monate bei CP B und CP C.
In der bislang umfangreichsten Studie von Pinter et al.4
wurden 59 mit Sorafenib behandelte Patienten untersucht, davon 23 mit Leberzirrhose CP B und 10 mit CP C. Es zeigte
sich ein medianes Follow-up von 8,3 Monaten bei CP A Patienten und ein medianes
Überleben von 4,3 Monaten bei CP B und nur 1,5 Monaten bei CP C.
Insgesamt traten vergleichsweise wenige
Nebenwirkungen auf, wobei die CP B/C-Gruppe vermehrt Grad 3 und 4-Nebenwirkungen
aufwies.
| Abou-Alfa3 | Wörns5 | Pinter4 | |
|---|---|---|---|
| CP A, keine Zirrhose | 9,4 Monate | 7,2 Monate | 8,3 Monate (medianes Follow-up) |
| CP B | 3,3 Monate | 3,3 Monate | 4,3 Monate |
| CP C | 3,4 Monate | 1,5 Monate |
Die bislang vorliegenden Überlebensdaten von Patienten mit fortgeschrittener Leberfunktionseinschränkung und Sorafenib-Therapie sind in der Tabelle 1 aufgeführt.
Child-Pugh C
Der Einsatz von Sorafenib bei Leberzirrhose im Stadium CP C erscheint aufgrund der schlechten Prognose der zugrundeliegenden Lebererkrankung nicht gerechtfertigt. Patienten im Stadium CP B mit 7 Punkten und nur leicht erhöhten Bilirubinwerten, gutem Allgemeinzustand ohne Aszites könnten eine Untergruppe darstellen, die ebenfalls von der Therapie profitiert. Eine individuelle Risikoabschätzung und Aufklärung des Patienten ist in jedem Fall notwendig.
1. Llovet, J.M. and J. Bruix, Molecular targeted therapies in hepatocellular carcinoma. Hepatology, 2008. 48(4): p. 1312-27.
2. Llovet, J.M., et al., Sorafenib in advanced hepatocellular carcinoma. N Engl J Med, 2008. 359(4): p. 378-90.
3. Abou-Alfa, G., et al., Is sorafenib (S) safe and effective in patients (pts) with hepatocellular carcinoma (HCC) and Child-Pugh B (CPB) cirrhosis? J Clin Oncol, 2008. 26 (May 20 suppl; abstr 4518).
4. Pinter, M., et al., Sorafenib in Unresectable Hepatocellular Carcinoma from Mild to Advanced Stage Liver Cirrhosis. Oncologist, 2009. 14(1): p. 70-76.
5. Wörns, M.A., et al., Safety and Efficacy of Sorafenib in Patients
With Advanced Hepatocellular Carcinoma in Consideration of Concomitant Stage of
Liver Cirrhosis.
J Clin Gastroenterol, 2009.





