Andrea Tannapfel, Bochum
Invasive Fibrosediagnostik
Die hohe klinische Relevanz der Leberbiopsie ist trotz erheblicher Fortschritte in der bildgebenden Diagnostik und in der Molekularbiologie ungebrochen, auch wenn Lebersteifigkeitsmessungen immer mehr Einzug in die klinische Routineüberwachung der Patienten mit chronischer Lebererkrankung nehmen. Die bildgebenden-apparativen „nicht-morphologischen“ Leberuntersuchungsmethoden haben den Vorteil der nicht invasiven Messung, die beliebig wiederholbar ist und z.B. auch an Assistenzpersonal delegiert werden kann. Vor dem Hintergrund steigender und zunehmend differenzierter therapeutischer Optionen ist jedoch eine kontinuierliche Anpassung auch der Leberbiopsie an den aktuellen Erkenntnisstand, eine Standardisierung der Befunde und vor allem eine Qualitätssicherung erforderlich, um den diagnostischen Nutzen der Leberbiopsie zu optimieren und ihren Einsatz zu rechtfertigen. In der Hand der erfahrenen Leberpathologen gilt die Leberbiopsie nach wie vor als Gold-Standard für die Diagnostik der Leberfibrose. Zusammen mit der makroskopischen Beurteilung der Leberoberfläche bei Laparoskopie können Sensitivität und Spezifität weiter gesteigert werden. In allen wesentlichen nationalen und internationalen Positionspapieren zur Leberbiopsie wird die histopathologische Untersuchung des Lebergewebes als richtige Maßnahme bei der Diagnostik von diffusen Lebererkrankungen (inklusive Autoimmunerkrankung, NASH und ASH) genannt. Insbesondere bei Patienten mit Zirrhose, bei denen in nahezu einem Drittel der Fälle eine Ätiologie nicht sicher festgestellt werden kann, ist die Leberbiopsie von unschätzbarem Wert.
Biopsiegröße
Im Gegensatz zur Elastografie kann durch die Biopsie nur ein 50.000tel der Leber untersucht werden. Dennoch wird empfohlen, insgesamt mehr als elf Portalfelder zu biopsieren, wobei aus eigener Erfahrung anzumerken ist, dass das Zählen der Portalfelder möglicherweise interindividuellen Schwankungen unterworfen sein kann. In vielen Studien zur Biopsiegröße ist nicht definiert, ob vollständige oder angeschnittene Portalfelder ausgewertet wurden. Durch Formalinfixation kann die Leberbiopsie eine Längsschrumpfung von bis zu 10 % zeigen. Daher sollte bei diffusen Lebererkrankungen die Biopsielänge von 1,5 cm nicht wesentlich unterschritten werden.
Die Analyse der Fibrose der Leber muss unter verschiedenen Aspekten diskutiert werden. Zunächst stellt sich die Frage, was unter Fibrose im nationalen und internationalen Schrifttum verstanden wird. Darüber hinaus gilt es zu hinterfragen, inwieweit die Fibrose von der Größe des Leberbiopsiezylinders abhängt. Definitionen und diagnostische Kriterien der Leberzirrhose und unterschiedliche Scoringsysteme der Leberfibrose müssen in die Bewertung mit einbezogen werden. Letztendlich gilt sich die Frage zu stellen, ob tatsächlich eine Zirrhose reversibel ist oder als unumgänglicher eindimensionaler Prozess zu verstehen ist.
Entstehung von Fibrose/Zirrhose
Die drei hauptsächlichen pathologischen Mechanismen, die zur Fibrose führen, sind Zelltod, Regeneration und konsekutive Fibrose (Narbenbildung).
Zelltod in der Leber kann als Folge jeglicher hepatozytärer Schädigung auftreten, der hepatozytäre Ersatz erfolgt so lange, bis die regenerative Kapazität des Lebergewebes erschöpft ist. In der normalen Leber findet sich interstitielles Kollagen, Typ 1 und 3 im Portaltrakt und um die Zentralvenen herum, zum Teil im Disse-Raum.
Während des progressiv fortschreitenden Fibroseprozesses bis hin zur Zirrhose kommt es zu einem Exzess von Typ 1 und Typ 3 Kollagen nicht nur innerhalb der Portalfelder, auch intralobulär, Septen entstehen. Parallel hierzu kommt es zu einer Konvertierung der Sinusoide in Kapillaren mit Basalmembran, was zu einer weiteren Hepatozytenschädigung führt, auch, weil z.B. Diffusionsbarrieren entstehen.
Kollagenvermehrung
Die Matrixproduktion erfolgt durch Hepatozyten, perisinusoidale Sternzellen und sinusoidale Endothelzellen. Der Hauptlieferant des exzessiven Kollagens während des Zirrhoseprozesses sind die perisinusoidalen Sternzellen. Fibrogenese wird durch eine ganze Reihe von chronischen inflammatorischen Mediatoren reguliert, so z. B. TNF-alpha oder beta, Interleukine und TGF-beta. Die vaskulären Veränderungen, die mit dem Fibroseprozess einhergehen, sind der pathophysiologische Schlüssel bei der Entstehung der Leberzirrhose. In der normalen Leber fehlt Endothelzellen die Basalmembran; kommt es zur Ablagerung extrazellulärer Matrix (Kollagen) im Disse-Raum, verschwinden die Fenestrierungen der Basalmembran durch die Matrixablagerungen. Parallel hierzu kommt es durch den fortschreitenden Prozess der Septenbildung zu einer Veränderung der Gefäßstrukturen der Portalregion und der terminalen hepatischen Gefäße, Blutshunts entstehen. Dabei führt die Zunahme der Fibrose und Sklerose der Portalfelder und ihrer Gefäßachsen zu einer präsinusoidalen Druckerhöhung. Fibrose der perivenulären Region kann den vaskulären Abfluss verhindern. Schreitet der Prozess weiter fort, kommt es zur Brückenbildung zwischen Portalfelder und Zentralvenen, portovenösen und arteriovenösen Shunts, die die Hepatozyten von den Gefäßen „abschnüren“. Liegt eine komplette Zirrhose vor, existiert ein ge-shunteter Blutfluss, der ganze Abschnitte hepatozytären Parenchyms umgeht. Die im Mikroskop sichtbaren Veränderungen gehören daher zur definitiven Diagnose einer Zirrhose und sind als diagnostisches Kennzeichen brauchbar.
Die morphologische Erscheinungsform der Leberzirrhose führte zur historischen Klassifikation in mikronoduläre und makronoduläre sowie gemischt noduläre Leberzirrhose. Dabei galt die Größe von 3 mm „Regeneratknotendurchmesser“ als Grenze bei der Differenzierung von mikro- und makronodulärer Leberzirrhose. Diese Einteilung ist heute weitestgehend verlassen, da die historisch gezogenen Rückschlüsse auf die Ätiologie so nicht mehr haltbar sind. So ist die Alkohol-induzierte Leberzirrhose zunächst mikronodulär, die Regeneratknoten können jedoch heterogen in der Leber mit der Zeit an Größe zunehmen, so dass eine makronoduläre oder gemischknotige Leberzirrhose entsteht. Die Einteilung in makro- und mikronoduläre Zirrhose ist daher weitestgehend verlassen.
Kontinuierlicher Prozess
Die Entstehung der Fibrose wird als kontinuierlicher Prozess verstanden. Wird die Zirrhose definiert als vollständige portoportale Septenbildung, vaskuläre Distorsion und Gallengangsproliferate scheint sie irreversibel zu sein. Allerdings können inkomplette Zirrhosen oder fortgeschrittene Fibrosen durchaus eine Regression zeigen. Die Matrixbildung ist ein dynamischer Prozess, man weiß, dass z.B. Kollagen 1 durch extensives Crosslinking resistenter gegenüber Kollagenasen wird. Die Leber selbst exprimiert eine ganze Reihe von Metalloproteinasen, so dass die Entstehung der Fibrose bzw. Zirrhose ein dynamischer Prozess ist, der nebeneinander fortschreitend oder regredient sein kann. Auch im Tiermodell konnte eine Rückbildung von fortgeschrittenen Fibrosestadien erreicht werden. Legt man allerdings die Trias aus Septenbildung, vaskulärer Distorsion und Gallengangsproliferaten der Diagnostik einer definitiven Zirrhose zugrunde, ist der Prozess morphologisch fixiert und irreversibel.
![Abbildung 1: Histologische Bilder mit unter- schiedlichen Fibrosegraden (F1 - F4) (Elastica-van-Gieson [EvG]).](images/fobi-tannapfel-1.jpg)
| Fibrosegrade F1 - F4 | ||
|---|---|---|
| A | F1 | milde/geringgradige Fibrose; keine Septen |
| B | F2 | mäßiggradige Fibrose; portale Faservermehrung |
| C | F3 | schwere/hochgradige Fibrose, zahlreiche Septen ohne Zirrhose |
| D | F4 | Zirrhose |
Abbildung 1: Histologische Bilder mit unter- schiedlichen Fibrosegraden (F1 - F4) (Elastica-van-Gieson [EvG]).
Definition
Im internationalen Schrifttum existieren keine allgemein akzeptierten Definitionen zur „Zirrhose“. Je nach Sichtweise und Fachdisziplin werden histopathologische Kennzeichen zusammen mit klinischen Parametern genannt (z.B. Narbenbildung und portalvenöser Hochdruck). Gemeinhin wird von einer chronisch-degenerativen Lebererkrankung gesprochen, bei der normales Lebergewebe zerstört wird und durch minderwertiges Narbengewebe ersetzt wird. Pathohistologisch sind für die definitive Zirrhosediagnostik folgende drei Kriterien zu fordern:
- Portoportal konfluierende Fibrosesepten,
- Gallengangsproliferationen und
- vaskuläre Alterationen (Kapillarisierung der Sinusoide, Shunts).
Dabei können diese Parameter unterschiedlich ausgeprägt sein, je nach Ätiologie der Leberzirrhose.
Insbesondere beim Vorliegen von sogenannten grobknotigen Leberzirrhosen gespielt die Biopsiegröße eine wesentliche Rolle. Wie bereits angeführt, gibt es keine international akzeptierten Empfehlungen, wie groß letztendlich die Biopsie sein muss, es wird davon ausgegangen, dass 12 bis 15 komplette Portalfelder in der Biopsie sichtbar sein sollten. Daraus resultiert eine maximale Biopsielänge von etwa 2 cm, der Durchmesser liegt bei 1,4 mm. Seit den Studien von Bedossa und Mitarbeitern (Hepatology 38, 1449 ff. 2003) ist unstrittig, dass die korrekte Klassifikation der Fibrose proportional mit der Biopsielänge zunimmt.
Klassifikation
In der Literatur existieren unterschiedliche Scoringsysteme, die das Vorhandensein oder Fehlen von Fibrosen mit einer metrischen Zahl belegen. Obwohl es sich bei der Entwicklung einer Leberfibrose um einen kontinuierlichen dynamischen Prozess handelt, der durch die Scoringsysteme in einen skalierten Punktescore überführt wird, sollten Klassifikationssysteme Verwendung finden, auch um die internationale Vergleichbarkeit zu sichern und eine präzise Einschätzung festzulegen.
Die unterschiedlichen Fibrosescores klassifizieren das Ausmaß der Fibrose sehr differenziert und belegen die Ausprägung mit Punktwerten von 0 (keine Fibrose) bis 4 bzw. 6 (wahrscheinliche, definitive Fibrose). Dabei sind die diagnostischen Kriterien festgelegt und sollen in der histopathologischen Befundbeschreibung genannt werden.
Eine derartig differenzierte, kategoriale Beschreibung gelingt mit den nicht-invasiven Fibrosemeßverfahren nicht.
Ein Problem der Leberbiopsie und Fibroseeinschätzung ist
die Beobachtung, dass der fibrotische Umbau des Lebergewebes nicht in allen
Fällen homogen verlaufen muss, so dass die Leberbiopsie hier eine
systemimmanente Fehlerquote in sich tragen kann. Wenn sich sonografisch
Hinweise auf derartige Inhomogenitäten ergeben, kann dieses (seltene) Problem
mit konsekutiven Biopsien des rechten und linken Leberlappens minimiert werden.
| Hepatitis-Activity (HAi-)Score | Metavir | Desmet und Scheuer | Knodell | Ishak-Score | |
|---|---|---|---|---|---|
| 0 | keine Fibrose | keine Fibrose | keine Faservermehrung | keine Fibrose | keine Fibrose |
| 1 | milde/geringgradige Fibrose | portale Faserve- mehrung | portale Faservermehrung keine Septen | portale Faservermehrung | Faservermehrung einiger Portalfelder mit oder ohne kurze Septen |
| 2 | mäßiggradige Fibrose | portale Faser- vermehrung mit vereinzelten Septen | inkomplette oder komplette portoportale Septen; erhaltene Architektur | keine Definition | Faservermehrung der meisten Portalfelder mit oder ohne kurze Septen |
| 3 | schwere/hoch gradige Fibrose | zahlreiche Septen ohne Zirrhose | septenbildende Faservermehrung Mit Architekturstörung, kein Anhalt Für kompletten zirrhotischen Umbau | portoportale oder portozentrale Septenbildung | portale Faservemehrung mit portoportalen Septen |
| 4 | Zirrhose | Zirrhose | wahrscheinliche oder definitive Zirrhose | Zirrhose | portale Faservemehrung mit ausgepräg- ten portoportalen oder portozentralen Septen |
| 5 | ausgeprägte Septenbildung (portoportal oder portozentral) mit einzelnen Knoten (inkomplette Zirrhose) | ||||
| 6 |
| wahrscheinliche oder definitive Zirrhose |
Tabelle 1: Vergleich der unterschiedlichen Fibrosescoring-Systeme.
Verschiedene Hepatitisformen
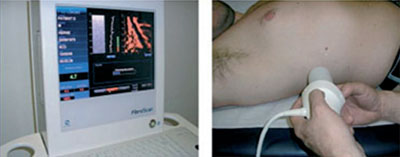
Abbildung 2: Messung der Leberdichte mit Fibroscan®.
| nicht invasive Verfahren | biopsie | |
|---|---|---|
| Erstdiagnose „Hepatitis“ | ---- | +++ |
| Verlaufskontrolle/ Prognose | +++ | + |
| Zirrhosediagnostik (F4) | ++ | +++ |
| Differenzierung F1 vs. F2 | + | +++ |
| Differenzierung F3 vs.F4 | + | +++ |
| Differenzierung F1 vs. F4 | +++ | +++ |
| Diagnose von Kofaktoren | ---- | +++ |
Tabelle 2: Diagnostischer Wert von Biopsie und nicht-invasiven Fibroseanalyseverfahren.
Der Verlauf der Virushepatitis kann hinsichtlich der Aktivität der Entzündung schwanken, die Entstehung der Fibrose / Zirrhose wird jedoch als relativ linearer Prozess zumindest bei Therapie-naiven Patienten verstanden. Die Entstehung der Fibrose beginnt portal, es zeigen sich kleine portale Fibroseareale, die im weiteren Verlauf portoportal konfluieren können, die Architektur ist in diesen Fällen noch erhalten. Bei schwerer oder hochgradiger Fibrose bilden sich Fasern, die bereits konfluieren und zu einer vereinzelten Knotenbildung führen. Liegt eine definitive Zirrhose vor wird gefordert, dass sich portoportal portozentale Septen ausgebildet haben, es kommt zu einer Architekturstörung, Zentralvenen sind nicht mehr sichtbar, als Folge der intrahepatischen Blutumverteilung entstehen Ektasien. Insbesondere zur Verlaufsbeurteilung eignen sich gerade bei Hepatitis B- und C-Virusinfektion daher die nicht-morphologischen Tests wie die Elastrografie. Allerdings können „Störfaktoren“, wie beispielsweise eine zusätzlich bestehende Leberzellverfettung (z.B. bei NASH) zu falschen Steifigkeitswerten führen. Darüber hinaus sind einige Virushepatitisinfektionen mit einer Virus-assoziierten Leberzellverfettung assoziiert (z.B. HCV - Genotyp 3). Auch hier zeigen sich nicht morphologische Verfahren der Leberbiopsie im Hinblick auf Fibroseeinschätzung unterlegen.
Allerdings sind auch die nicht-invasiven Verfahren, wie z.B. die Steifigkeitsmessung, nicht immer reproduzierbar und valide. Sie können nicht nur vom Untersucher abhängen, sondern auch von anderen Erkrankungen verzerrt werden. So werden besonders hohe Elastografie-Scores bei akuter Hepatitis, Rechtsherzbelastung oder auch Lebernekrosen gefunden. Dieser relativ häufigen Beobachtung bei akuter Hepatitis unterliegt die Leberhistologie naturgemäß nicht.
Die Autoimmunhepatitis zeichnet sich durch eine zumindest zum Krankheitsbeginn starke Entzündungsaktivität aus, in 25% der Fälle beginnt die Autoimmunhepatitis akut. In diesem Krankheitsstadium ist eine morphologische Fibroseanalytik in der Biopsie unentbehrlich, da hier zumeist das Ausmaß der Fibrose gering ist – und damit die Steifigkeitsmessungen nicht zu validen Ergebnissen führen. Die immer vorhandene floride Entzündung mit Gewebsödem bei akuter Hepatitis läßt ebenfalls eine nicht-morphologische Analytik nicht sinnvoll erscheinen.
Im Krankheitsverlauf der (unbehandelten) Autoimmunhepatitis kommt es kontinuierlich zum Rückgang der entzündlichen Aktivität, die Fibrose nimmt parallel hierzu zu. In diesem Stadium der Autoimmunhepatitis sind nicht morphologische Fibroseanalyseverfahren sicherlich zur Beurteilung der Fibrosedynamik sinnvoll.
Bei medikamentös-toxischen Leberschädigungen ist die Leberbiopsie sinnvoll, um eine Fibrose zu beurteilen. Zusätzlich können wichtige Differentialdiagnosen ausgeschlossen werden. Bei diesen Entitäten helfen elastografische Verfahren nur dann, wenn eine Zirrhose vermutet wird, insbesondere auch, wenn die in der Literatur gut etablierten Cut off-Werte signifikant überschritten werden.
Zur Differenzierung niedriger Fibrosestadien insbesondere bei nicht virologischen diffusen Lebererkrankungen bleibt die Leberbiopsie den transienten elastografischen Verfahren weiterhin deutlich überlegen. In diesem Kontext darf nicht übersehen werden, dass die Leberbiopsie neben der korrekten Einordnung des Stadiums der Erkrankung auch zusätzliche Informationen gibt (Entzündung, Verfettung, Cholestase).
Literatur bei der Verfasserin





