Hartwig Klinker, Würzburg
Medikamenten-Interaktionen mit Boceprevir und Telaprevir
Pharmakologische Interaktionen von zwei oder mehreren Medikamenten ergeben sich bei Nutzung identischer Transportersysteme sowie insbesondere im Bereich der Arzneimittel-abbauenden Enzymsysteme.
P-Glykoprotein
Das P-Glykoprotein (P-GP) stellt ein wichtiges zelluläres Transportprotein dar. Es ist ein Produkt des Multi Drug Resistance 1 (MDR 1)-Gens und wirkt ATP-abhängig als zelluläre „Efflux-Pumpe“. P-Glykoprotein weist eine hohe Substratspezifität für diverse, strukturell unterschiedliche Pharmaka auf und kommt in verschiedenen epithelialen Zellen u.a. des Endothels, im Darm, in der Niere, der Leber oder in Lymphozyten vor.
Im Gastrointestinaltrakt bewirkt P-Glykoprotein eine verminderte Absorption durch Zurückpumpen von Pharmaka in das Darmlumen. In der Leber führt P-GP zu einer verstärkten Elimination in die Galle, in der Niere wird die renale Eli-mination gefördert. Daneben wird P-GP im Bereich der Blut-Hirn-Schranke exprimiert und wirkt hier einer intracerebralen Penetration von Substanzen entgegen.
P-GP-Substrate sind u. a. diverse Zytostatika, Digoxin, Chinidin, Cyclosporin A, Tacrolimus, Ondansetron, Loperamid, Erythromycin, Levofloxacin, Dexamethason, Atorvastatin, Lovastatin, Diltiazem, Verapamil, Terfenadin, Ranitidin, Losartan, Morphin, Phenytoin oder Rifampicin. PGP kann induziert oder inhibiert werden. Die HCV-Protease-Inhibitoren Boceprevir und Telaprevir sind Inhibitoren des P-Glykoprotein. Komedikation, die P-GP-Substrate sind, werden also unter dem Einfluss von BOC oder TVR vermehrt resorbiert.
Cytochrom P450
Im Metabolismus diverser Phamaka spielt das Cytochrom P450-System (CYP), eine Gruppe mischfunktioneller Oxidasen mit über siebzig Isoenzymen, welches auch in der Darmmukosa, zum größten Teil aber in der Leber lokalisiert ist, eine herausragende Rolle. Einige wichtige CYP-Isoenzyme und Substrate sind in Abb. 1 dargestellt.
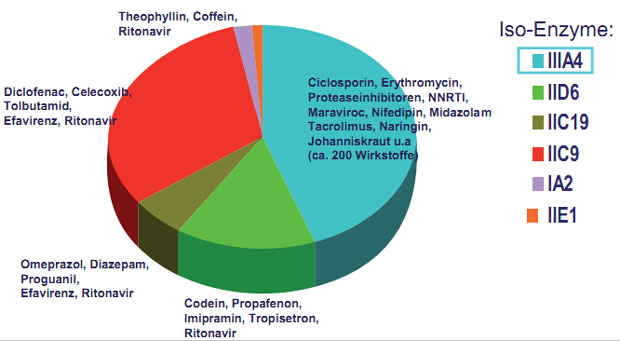
Abbildung 1: Cytochrom P450-isoenzyme und wichtige Substrate
Cytochrom-Isoenzyme unterliegen z. T. einem genetischen Polymorphismus und sind darüber hinaus in ihrer Funktionskapazität vielfältigen Einflüssen unterworfen.
Dabei kann es durch viele Pharmaka, die selbst Substrat des Cytochrom-Systems sind, zu einer Induktion oder Inhibition des Metabolismus kommen.
Eine Enzyminduktion führt zu einem rascheren Abbau von Substanzen mit der möglichen Folge eines Therapieversagens, eine Inhibition zu einem verzögerten Abbau mit der möglichen Folge einer Akkumulation der Substanz und vermehrter Toxizität.
Boceprevir und Telaprevir sind gleichzeitig Substrate und Inhibitoren des wichtigsten Isoenzyms CYPIIIA. Sie können daher mit anderen CYPIIIA-Substraten, CYPIIIA-Induktoren und CYPIIIA-Inhibitoren interagieren.
Nach Medikamenten fragen
Da viele der zu behandelnden Hepatitis C-Patienten eine Komorbidität mit der Notwendigkeit anderweitiger medikamentöser Therapien aufweisen, sind häufig pharmakokinetische Interaktionen mit den neuen HCV-Protease-Inhibitoren möglich.
Einer sorgfältigen Medikamentenanam-nese kommt daher große Bedeutung zu. Zu berücksichtigen sind dabei auch Genussmittel und pflanzliche Stoffe. So ist z. B. Johanniskraut ein potenter Induktor des CYPIIIA4, Naringin (ein Bestandteil in Grapefruitsaft) ein potenter Inhibitor.
Eine signifikante Bedeutung wird Änderungen der Fläche unter der Substanz- Konzentrations-Zeit-Kurve (AUC), die als Maß für die Medikamentenexposition angesehen wird, von mehr als 30 % beigemessen.
Boceprevir
Boceprevir wird an zwei CYPIIIA-Isoenzymen (A4 und A5) metabolisiert und unterliegt überwiegend einem anderweitigen Metabolismus durch Aldo-Keto-Reduktasen (AKR). Daher sind Interaktionen, insbesondere mit Beeinflussung der BOC-Phamakokinetik, in insgesamt geringerem Umfang als unter Telaprevir (s. u.) zu erwarten, jedoch nie auszuschließen. Interaktionsstudien mit Boceprevir wurden bislang in nur sehr geringem Umfang durchgeführt.
Die folgende Tabelle 1 zeigt bislang vermutete und bekannte Interaktionen mit Boceprevir. Eine Abweichung der AUC von > 30 % gegenüber der mit 100 % angesetzten AUC von Boceprevir ohne Komedikation ist in Zahlen angegeben.
Art und Ausmaß einer Interaktion von Boceprevir mit HIV-Protease-Inhibitoren sind unbekannt. In einer HIV-HCV-Koinfektions-Studie war der Einsatz der Nicht-Nukleosidischen Reverse Transkriptase-Inhibitoren Efavirenz, Etravirin und Nevirapin ein Ausschluss-kriterium (Sulkowski et al., 2011).
In vielen Fällen werden Dosismodifikationen der Komedikation empfohlen (s. Fachinformation).
Keine Interaktionen wurden bei einer Komedikation mit Tenofovir, Peg-Interferon α und Ribavirin gefunden.
Telaprevir
Telaprevir wird primär durch das CYP-IIIA metabolisiert.
Die folgende Tabelle 2 zeigt bislang vermutete und bekannte Interaktionen mit Telaprevir (eine Abweichung der AUC von >30 % gegenüber der mit 100 % angesetzten AUC von Telaprevir ohne Komedikation ist in Zahlen angegeben).
In vielen Fällen werden ebenfalls Dosismodifikationen der Komedikation empfohlen (s. Fachinformation).
Keine Interaktionen wurden bei einer Komedikation mit Esomeprazol gefunden.
Hervorzuheben sind neben der erheblichen Veränderung der Atorvastatin-Pharmakokinetik die Veränderungen im Metabolismus der Immunsuppressiva Cyclosporin und Tacrolimus. Bei einer Komedikation mit TVR erhöht sich die Cyclosporin-Exposition auf 460 %, gleichzeitig verlängert sich die Halbwertszeit von ca. 12 auf 40-50 Stunden. Diese ist bei Tacrolimus exorbitant auf ca. 200 Stunden verlängert, zusätzlich erhöht sich der Spitzenspiegel, der in der Regel mit der Toxizität einer Substanz korreliert, auf ca. das 10fache gegenüber einer Tacrolimus-Monotherapie.
Problematisch ist sowohl bei einer Therapie mit BOC als auch mit TVR eine Komedikation mit Benzodiazepinen. Hier ist für viele Substanzen mit einer Erhöhung der Konzentrationen und verlängerter Halbwertszeit zu rechnen, was bei der Anwendung dieser Substanzen als Sedativa im medizinischen Bereich (z. B. Schlafinduktion, Prämedikation in der Endoskopie, vor Eingriffen), aber auch im Rahmen eines eventuellen Beigebrauchs bei drogenabhängigen Patienten (z. B. bei der Substitution mit Opioidagonisten) eine Rolle spielen kann.
Tabelle 1: Interaktionen mit Boceprevir (oben) Tabelle 2: Interaktionen mit Telaprevir (rechts) |
|
HIV-Koinfektion
Pharmakokinetische Medikamenten-Interaktionen sind auch bei der Therapie der HIV-Infektion zu erwarten, da hier häufig mit Protease-Inhibitoren (PI), Nicht-Nukleosidischen Reverse Transkriptase-Inhibitoren (NNRTI) oder auch Maraviroc als einzigem bislang zugelassenen CCR5-Inhibitor CYPIIIA-Substrate eingesetzt werden.
| Atazanavir/r* | Telaprevir ↓, Atazanavir ↑ |
| Darunavir/r* | Telaprevir ↓ (65 %), Darunavir ↓ (60 %) |
| Forsamprenavir/r* | Telaprevir ↓(68 %), Amprenavir** ↓ (53 %) |
| Lopinavir/r* | Telaprevir ↓ (46 %) |
| Efavirenz | Telaprevir*** ↓, Efavirenz ↓ |
| Tenovir | Tenovir ↑ |
Tabelle 3: Interaktionen von Telaprevir mit antiretroviralen Medikamenten
* /r = HIV-Protease-Inhibitoren werden zur Verbesserung der Pharmakokinetik zusammen mit niedrig dosiertem Ritonavir (starker CYPIIIA-Inhibitor, „Booster“) gegeben
** Fosamprenavir ist Prodrug zu Amprenavir, gemessen wird Amprenavir
*** Telaprevir in erhöhter Dosierung von 3 x 1.125 mg/d!
Die bislang untersuchten Interaktionen von TVR (zu BOC liegen noch keine Daten vor) mit HIV-Medikamenten sind Tabelle 3 zu entnehmen (eine Abweichung der AUC von > 30 % gegenüber der mit 100 % angesetzten AUC von Telaprevir ohne Komedikation ist in Zahlen angegeben).
Unter den HIV-PIs treten die geringsten Interaktionen mit Atazanavir auf, bei einer Komedikation mit Efavirenz (CYPIIIA-Induktor) ist die TVR-Dosierung auf 3 x 1.125 mg/d zu steigern. Da die bislang als einziger HIV-Integrase-Inhibitor zugelassene Substanz Raltegravir keinem CYP-Metabolismus unterliegt, sind hier keine Interaktionen zu erwarten.
Insgesamt liegen zu Interaktionen mit den neuen HCV-Protease-Inhibitoren BOC und TVR bislang noch wenige Daten vor. Im Einzelfall sind daher Interaktionen auch mit anderen als den in dieser Übersicht genannten Substanzen nie auszuschließen!
Tipps für die Praxis
Eine große Bedeutung zur Erfassung möglicher Interaktionen kommt einer gewissenhaften Anamnese-Erhebung bezüglich bestehender Komorbiditäten und eingenommener Medikamente zu. Dabei ist auch an nicht verschreibungspflichtige sowie pflanzliche Medikamente zu denken. Zur möglichst lückenlosen Erfassung dieser Daten ist die Einbindung des Assistenzpersonals in der Praxis/Ambulanz häufig von großem Nutzen.
Jede Komedikation sollte vor Beginn einer Therapie mit BOC oder TVR nochmals auf den Prüfstand gestellt werden. Insbesondere ist zu prüfen, ob nicht einzelne Medikamente während der HCV-Therapie, die sich ja über einen absehbaren Zeitraum erstreckt, abgesetzt werden können oder zumindest vorübergehend verzichtbar sind.
Falls möglich, sind Instrumente zum
Monitoring der Komedikation zu nutzen. So besteht für verschiedene Medikamente
die Möglichkeit des Therapeutischen Drug Monitorings (TDM), wodurch konkrete
Veränderungen der Pharmakokinetik erkennbar werden. Etabliert ist ein TDM z. B.
für Immunsuppressiva, Antiepileptika, einzelne Antibiotika, Digitalispräparate
oder HIV-PI und -NNRTI. Für einige Substanzen ist es auch möglich,
Wechselwirkungen über Effektivitätskontrollen der Medikamente zu erkennen (z.
B. engmaschige Kon-trollen des Quick-Wertes bei Cumarin-Therapie).
| Antibiotika: | Betalactame |
| Antidepressiva: | Doxepin, Sertralin |
| Antidiabetika: | Metformin, Sulfonylharnstoffe, Insulin |
| Antiemetika: | Metoclopramid |
| Antiepileptika: | Levetiracetam |
| Antihistaminika: vCetiricin | |
| Antihypertensiva: | ACE-Inhibitoren, AT1-Inhibitoren, Betablocker |
| Atypische Neuroleptika: | Olanzapin |
| Diuretika: | Schleifendiuretika, Thiazide, Spironolacton |
| HIV- und HBV-Nukleosidanaloga | |
| HIV-Integrase-Inhibitor: | Raltegravir |
| Hypnotika: | Propofol |
| Koronarmittel: | Isosorbiddinitrat, Molsidomin |
| Lipidsenker: | Fibrate, Fluvastatin, Pravastatin |
| Migränemittel: | Rizatriptan |
| Neuropathiepräparate: | Gabapentin, Pregabalin |
| Nichtsteroidale | Antiphlogistika |
| Säureblocker: | Esomeprazol |
Tabelle 4: Substanzklassen und Substanzen mit geringem Interaktionspotential bei einer Komedikation mit Boceprevir oder Telaprevir
(Cave: für viele der aufgeführten Substanzen fehlen bislang pharmakokinetische Studien-Daten, in Einzelfällen können Interaktionen daher nicht ausgeschlossen werden!)
In den Fachinformationen von Victrelis® und Incivo® aufgeführte Kontraindikationen für bestimmte Medikamente in der Komedikation sollten beachtet werden.
Wegen der Vielfalt und auch der gelegentlichen Unvorhersagbarkeit möglicher Medikamenten-Wechselwirkun-gen ist die Nutzung von Interaktions-Datenbanken oft eine große Hilfe. Derartige Interaktions-Datenbanken zu HCV-Protease-Inhibitoren sind derzeit in Vorbereitung, verfügbar ist bereits die Datenbank der Universität Liverpool (Chair: Prof. D. Back) unter www.hep-druginteractions.org oder als App „HEP iCHART“.
Für wichtige Indikationsgebiete ist die Erstellung von Medikamenten-Austauschlisten wünschenswert, in denen Substanzen mit geringem Interaktionspotential gefunden werden können. Einige Substanzklassen und Einzelsubstanzen mit geringerem Interaktionspotential sind in der Tabelle 4 aufgeführt.
Weitere Studien zu konkreten Medikamenten-Interaktionen sind zur Erhöhung der Therapiesicherheit dringend erforderlich. Hier sind insbesondere auch die Hersteller der neuen Präparate gefordert.
Fazit
Mit der Zulassung der ersten direkt antiviral wirksamen HCV-Protease-Inhibitoren Boceprevir und Telaprevir hat eine neue Ära in der Hepatitis C-Therapie begonnen. Neu ist dabei auch das Risiko von Resistenzentwicklung und Medikamenten-Wechselwirkungen.
Sowohl BOC als auch TVR bergen aufgrund ihres Metabolismus ein Risiko, die Pharmakokinetik diverser anderer Substanzen zu verändern und unterliegen auch selbst Veränderungen der Pharmakokinetik. Dies kann zu unerwartetem Wirkverlust oder zu vermehrter Toxizität führen und ist damit von hoher klinischer Relevanz.
Interaktionen zwischen TVP/BOC und anderen Pharmaka sind im Einzelfall wenig vorhersagbar und können sich auch innerhalb derselben Substanzklasse unterscheiden.
Durch eine sorgfältige Anamneseerhebung, eine kritische und restriktive Verschreibungspraxis, die Nutzung von Datenbanken und die Erstellung von indikationsbezogenen Medikamenten-Austauschlisten ist die Problematik in aller Regel beherrschbar.
Zukünftige Therapieschemata werden auf dem Weg zu einer Interferon-freien Therapie zunehmend Kombinationen verschiedener HCV-Virustatika bein-halten. Gleichzeitig werden die zu be-handelnden Hepatitis C-Patienten älter mit entsprechend vermehrter Komor-bidität und Komedikation. Die hier durch zunehmende Problematik von Wechselwirkungen sollte Anlass zu intensiven Forschungsbemühungen auf diesem Gebiet sein.
Literatur
Boceprevir, Amerikanische Fachinformation
(prescribing information, Reference ID: 2946838, VictrelisTM), Mai 2011
Boceprevir, Fachinformation Victrelis®,
Stand Juli 2011
Garg V., Luo X., Alves K., Alexander l.,
Lee J.E., Lewis W., van Heeswiyk R., Kauffman R.S.. Significant Effect of the
Investigational HCV Protease Inhibitor Telaprevir on Cyclosporine and
Tacrolimus Pharmacokinetics.
Am Transplant Congress 2011: 65
Kasserra C., Hughes E., Treitel
M., Gupta S.,
and O‘Mara E..
Clinical Pharmacology of Boceprevir: Metabolism, Excretion, and Drug-Drug
Interactions.
18th CROI 2011: 118
Sulkowski M., Pol S., Cooper
C., Fainboim H.,
Slim j., Rivero A., thompson S., Greaves W.,
Wahl J., Mallolas J.. Boceprevir plus peg-Interferon/ribavirin for the
treatment of HCV/HIV co-infected
patients. Infectious Diseases Society of America (IDSA) 49th Annual Meeting
2001, LB-37
Telaprevir, Amerikanische
Fachinformation
(prescribing information, Reference ID: 2950502, IncivekTM), Mai 2011
Telaprevir, Fachinformation
Incivo®,
Stand September 2011
Telaprevir, Telaprevir NDA 201-917 FDA Advisory Committee Briefing
Document,
Vertex Pharmaceuticals, 28. April 2011
Van
Heeswijk R., Vandevoorde A., Boogaerts, G. Vangeneugden T.,De Paepe E.,
Polo R.,Van Solingen-Ristea R., De Backer K.,
Garg,V. and Beumont M.
Pharmacokinetic Interactions
Between Antiretroviral Agents and the Investigational HCV Protease Inhibitor
Telaprevir in Healthy Volunteers.
18th CROI 2011: 119





