Hepatitis C
Boceprevir bei HIV/HCV-Koinfektion
25. Oktober 2011
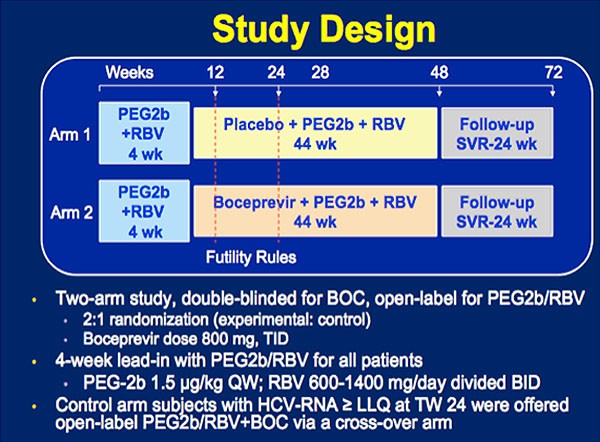
In der Pilot-Studie wurden 98 HCV-therapienaive Patienten entweder mit Tripletherapie (Boceprevir + pegIFN/RBV) oder konventionell (pegIFN/RBV) behandelt. Alle Patienten waren antiretroviral vorbehandelt (ungeboosterter PI, Raltegrvir, CCR-5-Antagonist, NRTI, kein NNRTI, kein AZT, kein d4T) und alle hatten eine HIV-RNA <50 Kopien/ml.
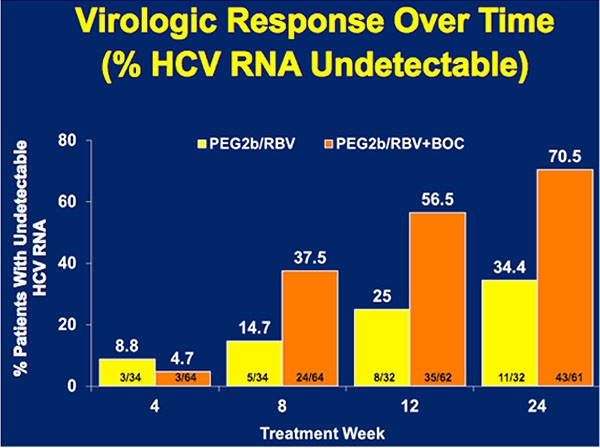
Nach dem 4wöchigen Lead-in hatten in der Boceprevir-Gruppe 8,8% vs. 4,7% keine nachweisbare HCV-RNA. Zu Woche 8 waren es in der Boceprevir-Gruppe 37% vs. 15%, zu Woche 12 56% vs. 25% und zu Woche 24 70% vs. 34%.
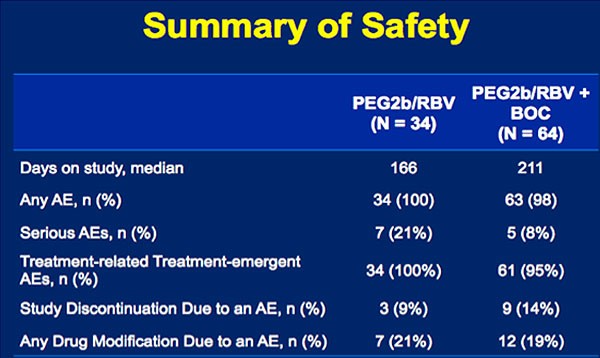
Bei den Nebenwirkungen waren folgende Ereignisse unter der Tripletherapie mit Boceprevir häufiger als unter
konventioneller Behandlung: Neutropenie (13% vs 3%), Geschmacksstörung (25% vs 15%), Erbrechen (25% vs 15%), Fieber (34%
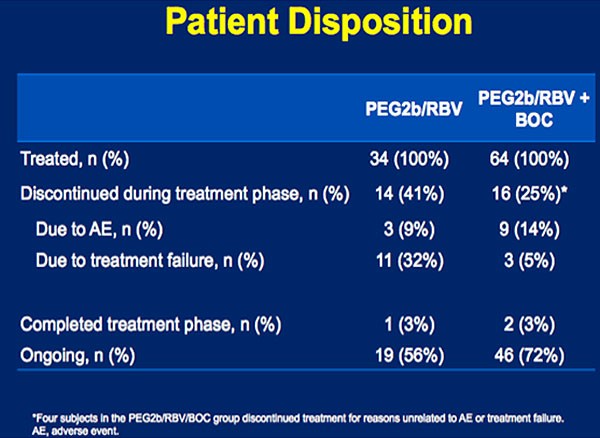
vs 21%), Kopfschmerzen (28% vs 12%) und verminderter Appetit (28% vs 12%). Mehr Patienten brachen die Studie wegen
unerwünschter Wirkungen ab (14% vs 9%). Schwere Nebenwirkungen waren unter Boceprevir jedoch seltener (8% vs 21%).