Hartwig Klinker, Würzburg
Neue DAA – neue Interaktionen?
Bei der Therapie mit DAA kann es zu gravierenden Wechselwirkungen kommen. Entsprechend ist Vorsicht geboten. Bei Fixkombinationen müssen alle Komponenten berücksichtigt werden.
Mit der Zulassung von Glecaprevir (G), Pibrentasvir (P) und Voxilaprevir (VOX) werden die Möglichkeiten zur Behandlung der chronischen Hepatitis C mit direkt antiviralen Substanzen (DAA = direct antiviral agent) nochmals deutlich erweitert. Glecaprevir und Voxilaprevir wirken als NS3/4A-Protease-Inhibitoren, Pibrentasvir als NS5A-Inhibitor.
Glecaprevir 100 mg und Pibrentasvir 40 mg sind als Fixkombination, die eine 1x tägliche Gabe ermöglicht (1x 3 Tabletten, entsprechend 300 mg G und 120 mg P), koformuliert (Handelsname Maviret®). Voxilaprevir 100 mg liegt ebenfalls als Fixkombination, zusammen mit Sofosbuvir 400 mg und Velpatasvir 100 mg, vor (Handelsname Vosevi®), die Dosierung ist 1x 1 Tablette/Tag. Beide Fixkombinationen sind pangenotypisch wirksam.
Im klinischen Alltag stellt sich nach Abschluss der Zulassungsstudien die Frage nach der klinischen Wirksamkeit der neuen Kombinationen in den unterschiedlichen HCV-Settings einschließlich des Vorliegens von Resistenz-assoziierten Varianten (RAVs), daneben nach dem Potenzial für Medikamenten-Wechselwirkungen (DDI = Drug Drug Interactions).
Der nachfolgende Artikel stellt die bisher vorliegenden Daten zu pharmakokinetischen Wechselwirkungen von Glecaprevir, Pibrentasvir und Voxilaprevir dar.
Hintergrund
Zu Wechselwirkungen kommt es insbesondere dann, wenn gleichzeitig eingenommene Medikamente dieselben Transportersysteme und/oder Metabolisierungsenzyme benötigen oder diese in ihrer Funktion modulieren. Im Metabolismus diverser Pharmaka spielt das Cytochrom P450-System (CYP) eine herausragende Rolle. Ca. 50% aller Medikamente werden allein über die Cytochrom-Subfamilie 3A4 verstoffwechselt. Zu berücksichtigen sind auch Genussmittel und pflanzliche Stoffe (z.B. Johanniskraut, Grapefruitsaft).
Eine Enzyminduktion führt zu einem rascheren Abbau von Substanzen mit der möglichen Folge eines Therapieversagens, eine Inhibition zu einem verzögerten Abbau mit der möglichen Folge einer Akkumulation der Substanz und vermehrter Toxizität.
Die Verteilung von Pharmaka in die einzelnen Kompartimente des Organismus hängt wesentlich von der Nutzung und Aktivität verschiedener Transporter ab, die als Influx- oder Efflux-Pumpen fungieren (Übersicht in Tab. 1).
CYP-Enzyme und verschiedene Transporter werden auch von den neuen HCV-DAAs genutzt und moduliert (Tab. 2).

Tab. 1 Wichtige Metabolisierungs-Enzyme und Arzneimittel-Transporter
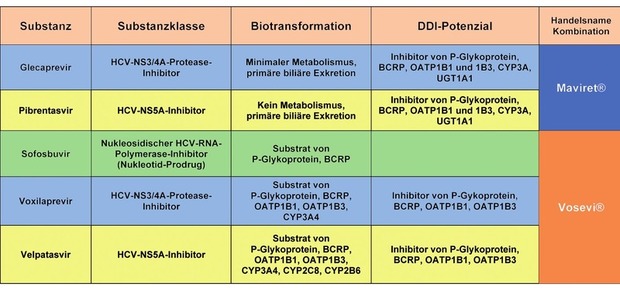
Tab. 2 Biotransformation und Wechselwirkungspotenzial der Glecaprevir, Pibrentasvir oder Voxilaprevir enthaltenden HCV-DAA-Fixkombinationen
Glecaprevir und Pibrentasvir werden nur geringfügig bzw. gar nicht hepatisch metabolisiert und sind daher selbst nicht ausgeprägten Wechselwirkungen unterworfen, inhibieren allerdings die Transporter P-Glykoprotein, BCRP sowie OATP1B1 und -1B3, daneben schwach Cytochrom3A und UGT1A1.
Voxilaprevir ist Substrat von CYP3A4 und CYP2C8, den Transportern P-Glykoprotein, BCRP sowie den OATPs. Die Substanz inhibiert P-Glykoprotein, BCRP sowie die OATPs1B1 und 1B3. Daraus ist abzuleiten, dass eine Glecaprevir-, Pibrentasvir- oder Voxilaprevir-haltige DAA-Kombination insbesondere zu Steigerungen der Substanzexposition einer Komedikation führen kann, die Substrat dieser Transporter ist. Da die neuen HCV-DAA nicht als Einzelsubstanzen verfügbar sind, sind zur Beurteilung des Wechselwirkungspotenzials immer auch die koformulierten Kombinationspartner mit zu berücksichtigen (s. auch Tab. 2). Generell ist mit einer klinischen Relevanz einer Interaktion zu rechnen, wenn die Substanzexposition um ca. >30% verändert wird.
Dieser Beitrag stützt sich allein auf – überwiegend in Abstractform – publizierte Daten sowie die Fachinformationen von Maviret® und Vosevi®. Interaktions-Datenbanken, die G/P oder VOX bereits berücksichtigen, liegen zum Zeitpunkt des Verfassens dieser Zeilen noch nicht vor. Insofern erhebt die Auflistung von Interaktionen keinerlei Anspruch auf Vollständigkeit.
Glecaprevir, Pibrentasvir und Voxilaprevir
In
den bisherigen Interaktionsstudien wurden eher modellhaft einige
Substanzen geprüft, die Substrat, Induktor oder Inhibitor bestimmter
CYP-Isoenzyme oder Transporter sind (Tab. 3 und 4) und damit ein
Potenzial besitzen, pharmakokinetische Wechselwirkungen mit G/P oder
VOX zu induzieren oder solchen unterworfen zu sein. Zu vielen, häufig
angewendeten und praktisch wichtigen Wirkstoffen liegen noch keine
Daten vor.
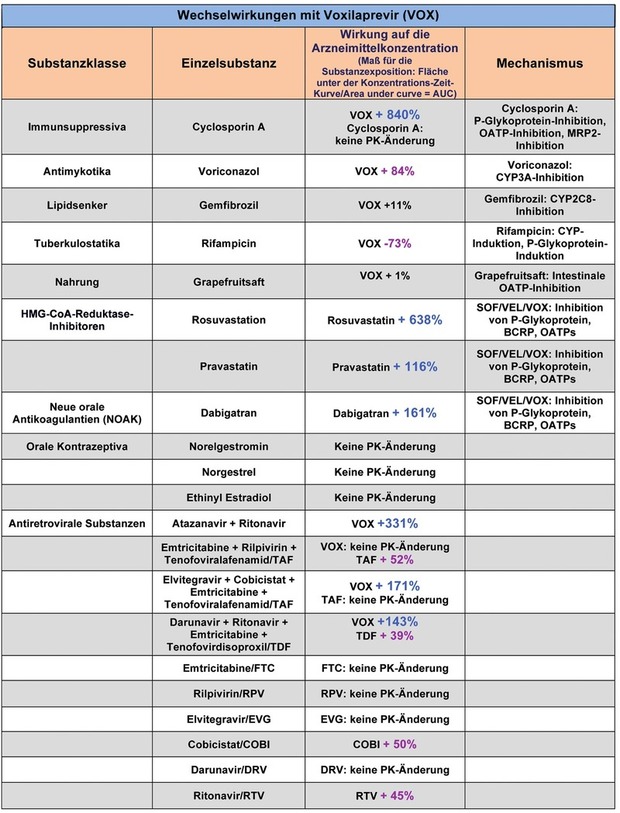
Tab. 3 Daten zu Wechselwirkungen mit Voxilaprevir Änderung der AUC um 31-100% Änderung der AUC um >100% PK = Pharmakokinetik
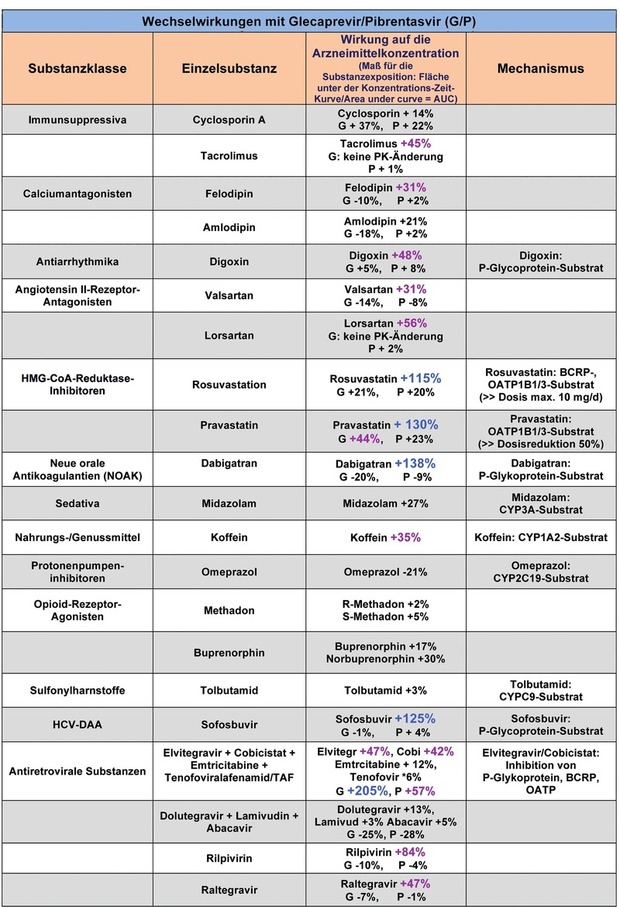
Tab. 4 Daten zu Wechselwirkungen mit Glecaprevir/Pibrentasvir (G/P) Änderung der AUC um 31-100% Änderung der AUC um >100% PK = Pharmakokinetik
Zu erwarten sind Beeinflussungen der Substanzexposition von G/P und/oder VOX generell durch weitere, die CYP- und/oder Transporter-Aktivität verändernde Medikamente.
Klassische Antiepileptika wie Carbamazepin, Phenobarbital oder Phenytoin sind starke Induktoren sowohl von CYP-Enzymen (3A4) als auch P-Gp, ähnlich verhält es sich mit Johanniskraut. Weitere CYP-Induktoren stellen die Tuberkulostatika Rifampicin, in geringerem Ausmaß Rifabutin und Rifapentin, das Glucocorticoid Dexamethason und die in der HIV-Therapie eingesetzten, älteren Nicht-Nukleosidischen Reverse Transkriptase-Inhibitoren Efavirenz, Etravirin und Nevirapin dar.
Wichtige Inhibitoren von CYP3A4 sind Makrolidantibiotika (Erythromycin, Clarithromycin, Telithromycin) mit der Ausnahme von Azithromycin, systemisch eingesetzte Antimykotika (Itraconazol, Ketoconazol, Posaconazol, Voriconazol) und antiretrovirale Therapieregime, die Ritonavir oder Cobicistat als pharmakokinetische Booster enthalten.
G/P
und VOX selbst inhibieren verschiedene Transporter und können so zu
einer Erhöhung der Konzentrationen einer Reihe anderer Wirkstoffe
führen. Zu den Substanzen und Substanzklassen, die diesbezüglich
gefährdet sind, zählen
Calciumantagonisten (z.B. Amlodipin,
Diltiazem, Nifedipin, Nisoldipin), HMG-CoA-Reduktase-Inhibitoren
(z.B. Atorvastatin, Rosuvastatin, Simvastatin, auch Pravastatin),
Antiarrhythmika (z.B. Digoxin, Flecainid, Mexiletin, Propafenon,
Amiodaron), Phosphodiesterase-5-Inhibitoren (Sildenafil, Tadalafil,
Vardenafil), Sedativa (z.B.
Midazolam oral), neue orale Antikoagulanzien (z.B.
Dabigatranetexilat), Antidepressiva (z.B. Sertralin, Mirtazapin,
Venlafaxin), DPP-4-Inhibitoren (z.B. Saxagliptin) und Neuroleptika
(z.B. Aripiprazol, Risperidon).
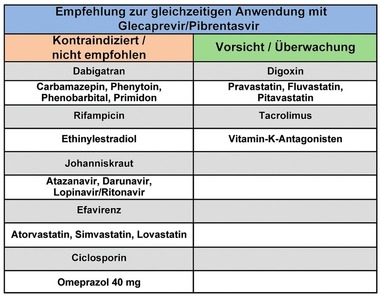
Tab. 5 In Kombination mit Glecaprevir/Pibrentasvir (G/P) kontraindizierte/nicht empfohlene sowie mit Vorsicht anzuwendende Medikamente
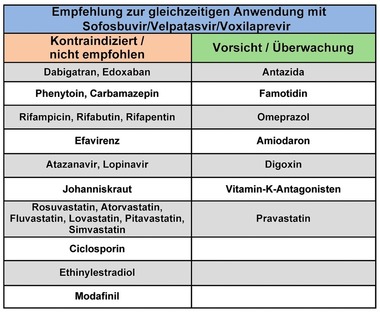
Tab. 6 In Kombination mit Sofosbuvir/Velpatasvir/Voxilaprevir (SOF/VEL/VOX) kontraindizierte/nicht empfohlene sowie mit Vorsicht anzuwendende Medikamente
Zu beachten ist, dass bislang nur sehr begrenzt Interaktionsdaten aus PK-Studien vorliegen und es sich bereits in der Vergangenheit wiederholt gezeigt hat, dass allein aus dem Metabolismus sowie Induktions- bzw. Inhibitionspotenzial der Einzelsubstanzen abgeleitete Wechselwirkungen klinisch oder in später durchgeführten PK-Studien anders bewertet werden mussten.
Aufgrund der verfügbaren Daten ist festzustellen, dass sich bislang keine Anhaltspunkte für ungewöhnliche Wechselwirkungen von G/P und VOX ergeben. Die in den aktuellen Fachinformationen mit den Bemerkungen „kontraindiziert / nicht empfohlen“ oder „Vorsicht/Überwachung“ versehenen Begleitmedikationen sind für G/P in Tab. 5 und für SOF/VEL/VOX in Tab. 6 dargestellt.
Empfehlungen
Im Management der Interaktionen gilt auch bei den neuen DAA:
- gewissenhafte Anamnese-Erhebung bezüglich bestehender Komorbiditäten und eingenommener Medikamente (auch nicht verschreibungspflichtige sowie pflanzliche Medikamente!).
- Jede Komedikation sollte vor Beginn einer Therapie mit DAA nochmals auf den Prüfstand gestellt werden. Insbesondere ist zu prüfen, ob nicht einzelne Medikamente während der HCV-Therapie, die sich ja über einen absehbaren Zeitraum erstreckt, abgesetzt werden können oder zumindest vorübergehend verzichtbar sind.
- Falls möglich, sind Instrumente zum Monitoring der Komedikation zu nutzen. So besteht für verschiedene Medikamente die Möglichkeit des Therapeutischen Drug Monitorings (TDM), wodurch konkrete Veränderungen der Pharmakokinetik erkennbar werden. Etabliert ist ein TDM z.B. für Immunsuppressiva, Antiepileptika, einzelne Antibiotika, Digitalispräparate oder HIV-PI und -NNRTI.
- Wegen der Vielfalt und auch der gelegentlichen Unvorhersagbarkeit möglicher Medikamenten-Wechselwirkungen ist die Nutzung von Interaktions-Datenbanken oft eine große Hilfe. Etabliert ist z.B. die Datenbank der Universität Liverpool (Chair: Prof. D. Back) unter www.hep-druginteractions.org oder als App „HEP iCHART“. Im Rahmen der ständigen Aktualisierung werden hier in Kürze auch Daten zu G/P und VOX verfügbar sein.
Garrison K. L., Kirby B., Stamm L. M. et al. Drug-drug interaction profile of sofosbuvir/velpatasvir/voxilaprevir fixed-dose combination. The Int. Liver Congress, 19-23 April 2017, Amsterdam/Netherlands, FRI-187
Garrison
K., Mogalian E, Zhang H et al. Evaluation of drug-drug interactions
between sofosbuvir/velpatasvir/voxilaprevir and boosted oor unboosted
HIV antiretroviral regimens. 18th Int. Workshop on Clin.
Pharmacol. of antiviral therapy, 14-17 june 2017, Chicago. O_20
Garrison K, Ma G, Stamm L et al. Lack of pharmacokinetic drug-drug interaction betweennorgestimate/ethinyl estradiol and sofosbuvir/velpatasvir/voxilaprevir. 18th Int. Workshop on Clin. Pharmacol. of antiviral therapy, 14-17 june 2017, Chicago. P_40
Kosloski MP, Dutta S, Ding B, Astryan A, Kort J, Liu W. Drug-drug interactions between next generation direct acting antivirals ABT-493 and ABT-530 with digoxin American Society for Clinical Pharmacology and Therapeutic (ASPCT) Annual Meeting, March 8-12, 2016, San Diego, CA
Kosloski MP, Dutta S, Ding B, Astryan A, Kort J, Liu W.Drug-drug interactions between next generation direct acting antivirals ABT-493 and ABT-530 with sofosbuvir. American Society for Clinical Pharmacology and Therapeutic (ASPCT) Annual Meeting; March 8-12, 2016: San Diego, CA
Kosloski MP, Dutta S, Pugatch D, et al. ABT-493 and ABT-530 combination demonstrated minimal potential for CYP-mediated drug-drug interaction. 51st Annual Meeting of the European Association for the Study of the Liver; April 13-17, 2016, Barcelona, Spain. Poster THU-229
Kosloski MP, Dutta S, Qi J, et al. Drug-drug interactions between direct-acting antivirals glecaprevir (ABT-493) and pibrentasvir (ABT-530) with angiotensin-II receptor blockers losartan or valsartan. 67th Annual Meeting of the American Association for the Study of Liver Diseases; November 11-15, 2016, Boston, MA. Poster 854
Kosloski MP, Dutta S, Zhao W, et al. Absence of significant drug-drug interactions between next generation direct acting antivirals ABT-493 and ABT-530 and methadone or buprenorphine/naloxone in subjects on opioid maintenance therapy. 66th Annual Meeting of the American Association for the Study of Liver Diseases; November 13-17, 2015, San Francisco, CA. Poster 723
Kosloski MP, Dutta S, Zhao W, et al. Drug-drug interactions between next generation direct acting antivirals ABT493 and ABT-530 with cyclosporine or tacrolimus in healthy subjects. 66th Annual Meeting of the American Association for the Study of Liver Diseases; November 13-17, 2015, San Francisco, CA. Poster 710
Kosloski MP, Viani RM, Qi X, Trinh R, Campbell A, Liu, W. Glecaprevir and pibrentasvir interactions with combination antiretroviral regimens. Conference on Retroviruses and Opportunistic Infections; February 13-16, 2017, Seattle, WA
Kosloski MP, Zhao W, Qaqish R, et al. Lack of significant drug-drug interactions between direct acting antivirals glecaprevir and pibrentasvir with calcium channel blockers (felodipine or amlodipine). American Society for Clinical Pharmacology and Therapeutics; March 15-18, 2017, Washington, DC
Kosloski MP, Zhao W, Li H, et al. Drug-drug interactions of glecaprevir and pibrentasvir with pravastatin, rosuvastatin, or dabigatran etexilate. 18th International Workshop on Clinical Pharmacology of Antiviral Therapy; June 14-17, 2017, Chicago, IL
Oberoi RK, Kosloski MP, Ding B, et al. Interactions between ABT-493 plus ABT-530 combination and rilpivirine or raltegravir. 23rd Annual Conference on Retroviruses and Opportunistic Infections; February 22-25, 2016, Boston, MA. Poster 453
Lin CW, Dutta S, Zhao W, Asatryan A, Campbell A, Liu W. Pharmacokinetic Interactions and Safety of Coadministration of Glecaprevir and Pibrentasvir in Healthy Volunteers Eur J Drug Metab Pharmacokinet. 2017 Jul 7. doi: 10.1007/s13318-017-0428-8. [Epub ahead of print]
Fachinformation Vosevi®, Stand Juli 2017
Fachinformation Maviret®, Stand Juli 2017





