Livermeeting® 2011*
Subanalyse von Phase III-Studie mit Telaprevir
In den Zulassungsstudien war die Telaprevir-basierte Tripletherapie der bisherigen Standardtherapie aus pegyliertem Interferon alfa und Ribavirin (PR) signifikant überlegen. So erreichten 79 % der therapienaiven Patienten in der Studie ADVANCE mit der Tripletherapie ein anhaltendes virologisches Ansprechen (SVR) im Vergleich zu 46 % der Patienten mit PR (p < 0,0001). 1 Und je nach Ansprechen auf die zuvor erfolglose PR-Therapie – Relapser, partielle Responder und Nullresponder – erzielten in der Studie REALIZE 84 %, 61 % und 31 % im Vergleich zu 22 %, 15 % und 5 % der vorbehandelten Patienten eine SVR (je p < 0,0001). 1 Insgesamt 58 % der thera-pienaiven Patienten in ADVANCE und 76 % der Relapser in REALIZE sprachen auf die Tripletherapie früh an (eRVR: HCV-RNA zu Woche 4 und 12 nicht nachweisbar). 2 Gemäß der Zulassung kann mit einer Telaprevir-basierten Trip-letherapie sowohl bei therapienaiven Patienten als auch bei Relapsern mit eRVR die gesamte Behandlungszeit auf 24 Wochen verkürzt werden (12 Wochen Triple-Therapie gefolgt von 12 Wochen PR). 1 Alle anderen Patienten werden 48 Wochen lang behandelt (12 Wochen Trip-le-Therapie, gefolgt von 36 Wochen PR).
Hohe SVR-Raten bei Relapsern
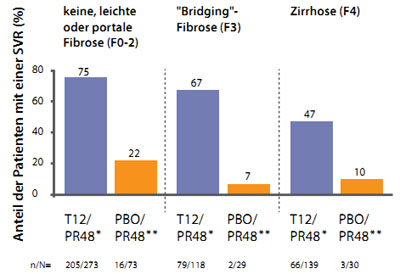
Abbildung 1: REALIZE: SVR nach Fibrosegrad zu Studienbeginn (erst. nach Pol S et al. AASLD 2011; Abstract #31)
* gepoolte Daten der beiden Studienarme12 Wochen Tripletherapie plus 36 Wochen PR mit und ohne Lead-in-Phase
** Plazebo/48 Wochen PR
Eine aktuelle Subanalyse der Studie REALIZE ergab, dass die Tripletherapie mit Telaprevir auch bei HCV-infizierten Patienten mit einhergehender kompensierter Zirrhose im Vergleich zur PR-Therapie deutlich höhere Heilungsraten erzielt (47 % vs. 10 %; Abb.). 3 Die Sub-analyse umfasst die Daten von 530 Patienten, von denen bei 139 eine Zirrhose (F4) diagnostiziert wurde. Vorherige Relapser mit Zirrhose erreichten die höchsten SVR-Raten (84 % vs. 7 %), gefolgt von den vorherigen partiellen Respon-dern (34 % vs. 20 %) und den vorherigen Nullrespondern (14 % vs. 10 %). Die unerwünschten Ereignisse stimmten mit denjenigen, die in den klinischen Studien der Phase III berichtet wurden, überein. Hautauschlag (Rash), Juckreiz und Anämie traten bei HCV-Patienten mit zirrhotischer Leber, die Telaprevir erhielten, häufiger auf als bei PR alleine.
Vorheriges Ansprechen prädiktiv
In der REALIZE-Studie hatte eine vor-geschaltete Lead-in-Phase keinen Effekt auf den Erfolg der Tripletherapie mit Telaprevir. 1 Eine weitere Analyse dieser Studie bestätigt nun, dass das Ansprechen auf eine vorangegangene Behandlung ein genauerer Indikator für einen Heilungserfolg mit Telaprevir sein kann als das virologische Ansprechen nach einer vierwöchigen Lead-in-Phase alleine. 4 Analysiert wurde die Viruslast zu Woche 4 von 121 Patienten aus dem PR-Arm und 239 Patienten aus dem Tripletherapie-Arm mit Lead-in. Sprachen die Patienten gleichermaßen schlecht auf die Lead-in-Phase an (Viruslastabfall 0-0,5 Log-Stufen), erzielten trotzdem viele vorherige Relapser und partielle Responder eine SVR (67 % und 60 %), aber nur wenige vorherige Nullresponder (6 %).
1 Aktuelle Fachinformation Incivo®
2 Prescribing Information Incivek®, Stand Mai 2011
3 Pol S et al. AASLD 2011; Abstract #31
4 Zeuzem S et al. AASLD 2011; Abstract #1331
* 62nd Annual Meeting of the American Association of the Study of the Liver (AASLD), 4.-8. November 2011 in San Francisco/USA
Mit freundlicher Unterstützung der Janssen-Cilag GmbH, Neuss
Autorin:
Andrea Warpakowski, Itzstedt





