Klaus Stark1, Judith Koch1, Wolfgang Jilg2, Ole
Wichmann1
Hepatitis E – Epidemiologie und Risikofaktoren in Deutschland
Meldedaten nach Infektionsschutzgesetz (IfSG)
HEV-Infektionen sind in Deutschland seit 2001 nach Infektionsschutzgesetz (IfSG) meldepflichtig. Seither stieg die Anzahl der übermittelten HEV-Fälle kontinuierlich an (Abb. 1). Im Jahr 2009 wurden dem RKI insgesamt 108 Hepatitis-E-Erkrankungen gemäß Referenzdefinition übermittelt. Beim Vergleich der autochthonen und importierten Fälle ist erkennbar, dass der Anstieg der Meldezahlen in den letzten Jahren nur die autochthonen HEV-Fälle betrifft (Abb. 1). Für das Jahr 2009 lagen von 103 Erkrankten Angaben zum möglichen Infektionsland vor. Von den 104 Nennungen entfielen 81% auf Deutschland (2008: 69%). Wie schon in den Vorjahren waren auch 2009 Männer mit einem Anteil von 67% (n=72) an allen Hepatitis-E-Fällen häufiger betroffen als Frauen. Ein großer Teil (75%, n=81) entfiel auf die Altersgruppen der 30- bis 69-Jährigen. Unter den seit 2001 übermittelten Fällen sind in beiden Gruppen 65% der Fälle männlichen Geschlechts. Eine Dominanz von Männern und älteren Personen unter den autochthonen HEV-Fällen wurde auch in anderen europäischen Ländern wie zum Beispiel in England oder den Niederlanden beobachtet.13,14
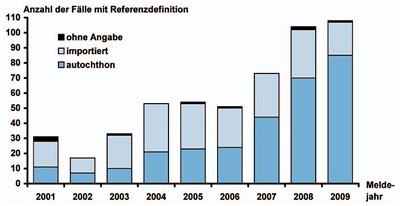
Abb. 1: Hepatitis-E-Erkrankung in
Deutschland, 2001 bis 2009 (übermittelt an das RKI gemäß Infektionsschutzgesetz)
Serologische Surveys und Studien bei Personen mit unklarer Hepatitis belegen, dass Hepatitis E eine deutlich unterdiagnostizierte Krankheit in Europa ist, insbesondere bei Patienten mit negativer Reiseanamnese.7,15
Fall-Kontroll-Studie 2006–2007
Vom 1. Mai 2006 bis zum 31. August 2007 führte das RKI in Zusammenarbeit mit den Landesstellen und Gesundheitsämtern und der Abteilung Klinische Virologie und Infektionsimmunologie der Universität Regensburg eine Fall-Kontroll-Studie mit zusätzlichen molekularbiologischer Typisierung von HEV-Stämmen durch. Die Studie sollte Daten zu wichtigen Übertragungswegen und Risikofaktoren bei den autochthonen Fällen liefern. Die Ergebnisse dieses Projekts wurden veröffentlicht und sollen hier noch einmal zusammenfassend dargestellt werden.16,17
Wesentliche Ergebnisse
In dem 16-monatigen Studienzeitraum konnten 76 HEV-Fälle mit klinischen Symptomen befragt werden. Von 47 (62%) konnten Stuhl- oder Blutproben asserviert und ins Konsiliarlabor versandt werden. Fünf Fälle wurden im weiteren Verlauf ausgeschlossen, da sowohl die PCR-Untersuchung als auch der serologische Bestätigungstest mittels IgM-Westernblot negativ waren. Fünf weitere Fälle wurden ausgeschlossen, da diese als Sekundärfälle in zwei Haushalten auftraten. In der endgültigen Datenanalyse wurden somit 66 HEV-Fälle berücksichtigt: 45 (68%) mit autochthoner und 21 (32%) mit importierter HEV-Infektion. Wie auch aus den Meldedaten ersichtlich, handelte es sich bei den meisten autochthonen (76%) und importierten (62%) HEV-Fällen um Männer, wobei das Alter der autochthonen Fälle signifikant höher war (Median: 46 Jahre im Vergleich zu 37 Jahren bei den importierten Fällen). Ein wesentlicher Unterschied bestand auch in der Wohnortgröße. Während 51% der autochthonen Fälle in Ortschaften mit weniger als 20.000 Einwohnern lebten, waren nur 5% der importierten Fälle in Ortschaften dieser Einwohnergröße wohnhaft. Klinisch bestanden keine Unterschiede zwischen autochthonen und importierten Fällen. Stationär im Krankenhaus behandelt werden mussten 78% der autochthonen und 62% der importierten Fälle.
Von den importierten HEV-Fällen hatten sich mehr als 50% auf dem indischen Subkontinent aufgehalten. Andere Reiseregionen waren Afrika (24%), Südostasien (14%) und die Karibik (5%). Ein hoher Anteil von Personen mit im Ausland erworbener HEV-Infektion hatte auf der Reise in eher bescheidenen Unterkünften übernachtet (67%) und während des Aufenthalts Risikoprodukte für gastroenterale Erkrankungen konsumiert (71% Salat, 38% Eiswürfel, 29% Leitungswasser).
Phylogenetische Analysen
Von 24 HEV-Fällen konnte der Erreger isoliert und sequenziert werden. Bei 8 (89%) von 9 importierten HEV-Stämmen handelte es sich um Genotyp 1. Sieben der Stämme waren vom indischen Subkontinent importiert und einer aus Äthiopien. Bei einem aus den USA importierten Stamm handelte es sich um einen Genotyp 3.
Bei 14 von 15 autochthonen HEV-Stämmen handelte es sich um Genotyp 3. Bei dem anderen autochthonen Fall konnte ein Genotyp 4 nachgewiesen werden. Bislang war dieser Genotyp nur in Asien nachgewiesen worden. Eine Studie in Japan legt die Vermutung nahe, dass Patienten mit Genotyp-4-Infektionen tendenziell schwerere klinische Manifestationen entwickeln als Patienten, die mit dem HEV-Genotyp 3 infiziert sind.18 Weitere molekular-epidemiologische Studien sollten unternommen werden, um zu klären, ob Genotyp 4 tatsächlich bereits in Europa zirkuliert oder ob der in dieser Studie beobachtete Genotyp 4 nur singulär zum Beispiel über ein Nahrungsmittelprodukt oder einen Reisenden importiert worden war. In der phylogenetischen Analyse der autochthon erworbenen Genotyp-3-Stämme zeigte sich, dass bei den meisten eine hohe Sequenz-Übereinstimmung mit HEV-Stämmen bestand, die vornehmlich in den Niederlanden bei Schweinen isoliert worden waren.
Risikofaktoren
Für die Fall-Kontroll-Studie konnten neben den 45 oben beschriebenen autochthonen HEV-Fällen 135 individuell gemachte Kontrollen rekrutiert und befragt werden. In bivariater Analyse war der Verzehr folgender Nahrungsmittel innerhalb von 2 Monaten vor Symptombeginn signifikant (p-Wert < 0,05) mit dem Auftreten einer HEV-Infektion assoziiert: Innereien (41% der Fälle vs. 19% der Kontrollen), Wildschwein (20% vs. 7%) und rohes bzw. nicht ganz durchgegartes Rindfleisch (31% vs. 14%). Der Besitz von Haustieren, insbesondere von Katzen (9% der Fälle vs. 27% der Kontrollen), war negativ assoziiert mit autochthoner HEV-Infektion.
Folgende Faktoren waren in unserer Studienpopulation nicht mit einer autochthonen HEV-Infektion assoziiert und hatten bei geringer Prävalenz auch keine wesentliche Bedeutung: Leben oder Arbeiten auf einem landwirtschaftlichen Hof (4% der Fälle vs. 4% der Kontrollen), berufliche Exposition zu Tieren (4% vs. 5%), direkter Kontakt zu Schweinen (2% vs. 2%), Besitz von Nutztieren (2% vs. 7%) sowie Bluttransfusion (0% vs. 0%), Kontakt zu Oberflächenwasser (13% vs. 16%) und direkter Kontakt zu Abwasser (2% vs. 0,7 in den letzten 2 Monaten vor dem Erkrankungszeitpunkt.
In multivariater Analyse (mittels konditioneller logistischer Regression) war der Verzehr von Innereien (OR 2,7; 95% KI 1,2-6,2) und Wildschwein (OR 4,3; 95% KI 1,2-15,9) in den 2 Monaten vor Symptombeginn unabhängig mit dem Auftreten einer autochthonen HEV-Infektion assoziiert. Betrachtet man die beiden Risikofaktoren kombiniert, so hatten 53% der HEV-Fälle eines der beiden Produkte vor der Erkrankung verzehrt im Vergleich zu 24% der Kontrollen im gleichen Zeitraum (adjustierte OR 3,5; 95% KI 1,8-7,7). Die negative Assoziation mit dem Besitz von Haustieren (OR 0,4; 95% KI 0,17-0,95) blieb auch in der multivariaten Analyse bestehen.
Von den 21 HEV-Fällen (47%), die weder Innereien noch Wildschwein verzehrt hatten, gaben 14 (67%) an, in den zwei
Monaten vor der Erkrankung rohes oder nicht ausreichend gegartes Schweinefleisch verzehrt zu haben, was aber nicht
signifikant häufiger war als unter Kontrollen. Keiner der 21 Fälle hatte direkten Kontakt zu
Tieren.
Zusammenfassung
Die Ergebnisse der Fall-Kontroll-Studie und der phylogenetischen Untersuchungen, die im Rahmen der intensivierten HEV-Surveillance erfolgten, zeigen, dass die Hepatitis E in Deutschland endemisch als Zoonose existiert und das Virus wahrscheinlich bei einem erheblichen Teil der autochthonen Erkrankungsfälle durch den Verzehr von Fleisch- und Innereiprodukten übertragen wird.
Fast alle untersuchten HEV-Isolate von autochthonen Fällen aus ganz Deutschland gehörten zum Genotyp 3 mit großer Sequenzähnlichkeit zu HEV-Isolaten, die bei Schweinen in den Niederlanden nachgewiesen wurden.17 HEV-Genotyp 3 wurde mittlerweile in Deutschland auch in Seren und in Leberproben von Wildschweinen nachgewiesen.19,20,21 Aber auch in anderen europäischen Ländern verdichten sich die Hinweise, dass HEV in Tierpopulationen zum Teil stark verbreitet ist: In einer Population von Wildschweinen in Italien wurde das Virus bei 25% der Tiere nachgewiesen, auf einer kommerziellen Schweinefarm in Spanien schieden 17% der Tiere das Virus aus.4,22 In den Niederlanden wurde das Virus in 6,5% von kommerziell erhältlichen Schweinelebern nachgewiesen und das Isolat konnte – vermutlich dosisabhängig – wiederum Schweine infizieren.23 In allen drei Studien war ausschließlich HEV-Genotyp 3 nachgewiesen worden.
Bei der hier beschriebenen Fall-Kontroll-Studie handelt es sich um die erste populationsbezogene analytische Studie zu Risikofaktoren einer Hepatitis E in einem Industrieland. Der Nachweis von HEV-Genotyp 3 in Schweinepopulationen legte zwar schon die Vermutung nahe, dass diese als Infektionsquelle für den Menschen in Betracht kommen, es hätte aber auch ein anderes Tierreservoir existieren können, das für beide, Mensch und Schwein, eine Infektionsquelle darstellt. Die Fall-Kontroll-Studie zeigt, dass der Konsum von Innereien und Wildschwein einen für den Menschen bedeutenden Übertragungsweg in Deutschland darstellt. Jedoch konnten nur ungefähr 53% der Erkrankungen durch diesen Konsum erklärt werden. Als mögliche andere Infektionsquelle könnte unter anderem nicht ausreichend gegartes Schweinefleisch in Frage kommen. Zur Beantwortung dieser Frage sind weitere Studien erforderlich. In der Tat meinten 79% der Fälle sich zu erinnern, rohes oder nicht ausreichend gegartes Schweinefleisch in den zwei Monaten vor der Erkrankung gegessen zu haben, aber auch 66% der Kontrollen.
Für eine Infektion beim Menschen durch den Verzehr von Fleischprodukten müssen (abgesehen von der Möglichkeit der Kreuzkontamination durch andere Lebensmittel) zwei eher seltene Ereignisse zusammentreffen: Das Fleisch muss mit initial ausreichend HEV kontaminiert sein und der Gar- oder Bratvorgang muss so kurz sein, dass das Virus in einer infektiösen Dosis überlebt. Dies könnte zum Teil erklären, warum generell so wenig Hepatitis-E-Fälle in Europa auftreten, wobei nicht vergessen werden darf, dass ein nicht unerheblicher Teil von Infektionen wahrscheinlich asymptomatisch oder sehr mild verläuft und ein Teil der symptomatischen Erkrankungen nicht diagnostiziert wird. Die Fall-Kontroll-Studie schließt andere Übertragungswege nicht aus. Es ist durchaus vorstellbar, dass eine direkte orale Aufnahme des HEV auch über kontaminiertes Oberflächenwasser oder Abwasser oder auch durch direkten Kontakt mit kontaminiertem Tierkot erfolgen kann. Diese Übertragungswege sind wie auch die parenterale Übertragung während chirurgischer Eingriffe an Tieren durchaus möglich, spielen aber zumindest in Deutschland – wie in der Fall-Kontroll-Studie gezeigt – keine wesentliche Rolle. In Frankreich wurde vor kurzem ein Fallbericht über einen Studenten publiziert, der sich beim chirurgischen Training an einem Schwein mit HEV infiziert hatte.24
Die negative Assoziation zwischen Katzenbesitz und autochthoner HEV-Infektion ist weitgehend unklar. Der Besitz von
Haustieren bzw. Katzen könnte einen Effekt auf das Fleischkonsum-Verhalten der Befragten gehabt haben. Alternative
Hypothesen könnten sein, dass Katzenbesitzer häufiger immun sind durch früher durchgemachte subklinische Infektionen,
die aufgrund regelmäßiger Zubereitung von Leber als Katzenfutter erfolgt sein könnten, oder dass der Haushalt von
Katzenbesitzern normalerweise frei von Nagetieren ist. Die Rolle von Nagetieren bei der Übertragung von HEV ist noch
nicht vollständig geklärt. Das Virus konnte bislang nicht von Nagetieren isoliert werden, dafür konnten aber erstaunlich
hohe IgG-Antikörperprävalenzen in Nagetierpopulationen in den USA nachgewiesen
werden.25
Fälle und Kontrollen waren nach Alter, Geschlecht und Wohnortgröße gemacht, so dass diese drei Faktoren nicht als Risikofaktoren in der Analyse betrachtet werden konnten. Der signifikante Altersunterschied zwischen importierten und autochthonen Fällen mag auch darin begründet sein, dass jüngere Menschen häufiger unter einfachen hygienischen Bedingungen reisen und auf Reisen auch im Essverhalten höhere Risiken eingehen. Zudem kann vermutet werden, dass eine höhere Prävalenz von Leber- oder anderen Grunderkrankungen zu der Tatsache führt, dass mehr ältere Personen und mehr Männer mit einer autochthonen HEV-Infektion diagnostiziert und übermittelt werden. Bei Personen mit entsprechenden Leber-Grunderkrankungen können sich theoretisch HEV-Infektionen schwerer manifestieren und so zur Meldung kommen. Alternativ kann auch vermutet werden, dass ein unterschiedliches Fleisch-Konsumverhalten dieser Personengruppe ebenfalls zu einer höheren Infektionshäufigkeit führt.
Empfehlung
Hepatitis E ist eine seltene in Deutschland übermittelte Infektionskrankheit. Jedoch hat die Anzahl der Meldungen in den letzten Jahren kontinuierlich zugenommen, was fast ausschließlich durch einen Anstieg der autochthonen Fälle bedingt war. Ärzte sollten auch bei negativer Reiseanamnese bei einer akuten Hepatitis eine HEV-Infektion differenzialdiagnostisch in Betracht ziehen. Bei älteren Personen mit Leber-Grunderkrankungen scheinen sich HEV-Infektionen häufiger symptomatisch, zum Teil auch schwerer zu manifestieren.
Phylogenetische Untersuchungen und Studien bei Schweinen und Wildschweinen liefern inzwischen klare Belege dafür,
dass die Hepatitis E als eine Zoonose in Industrieländern besteht, wobei hier überwiegend der Genotyp 3 übertragen wird.
In Industrieländern scheinen zumindest Schweine und Wildschweine ein wesentliches Reservoir und auch eine direkte
Infektionsquelle zu sein. Der Verzehr von vermutlich nicht ausreichend gegarten Innereien oder Wildschweinfleisch konnte
in der Fall-Kontroll-Studie als Risikofaktor in Deutschland identifiziert werden. Bei der Zubereitung dieser
Fleischprodukte sollten entsprechende hygienische Maßnahmen eingehalten werden. Zum einen sollten Kreuzkontaminationen
mit anderen Nahrungsmitteln, die dann später nicht mehr gekocht werden, vermieden werden. Zum anderen sollten die
Fleischprodukte nicht in einem rohen oder halbrohen Zustand konsumiert werden, sondern bei ausreichend hohen
Temperaturen gegart werden.26
Literatur bei den Verfassern





