Tobias Müller1,
Jonas Rosendahl2 und Thomas Berg2, Leipzig
IL28B Update 2010
Der Erfolg einer Interferon (IFN)-α basierten Kombinationstherapie bei chronischer Hepatitis C Virus (HCV)-Infektion wird maßgeblich von viralen Faktoren wie z.B. HCV-Genotyp und initialer Viruslast sowie epidemiologischen bzw. klinischen Wirtsfaktoren wie z.B. Alter, Geschlecht, und Ethnizität des Patienten sowie dem Ausmaß der hepatischen Fibrose beeinflusst. Die frühe Viruskinetik nach Therapiebeginn gibt Aufschluss über die individuelle Therapie-Suszeptibilität und spielt daher eine entscheidende Rolle bei der Planung der Therapiedauer („Response-gesteuerte Therapie“). Hierbei hat sich insbesondere die rasche und komplette Suppression der Hepatitis C-Virämie unter die Nachweisgrenze sensitiver Tests innerhalb der ersten 4 Wochen nach Therapiebeginn (rapid virological response, RVR) als wichtigster positiver prädiktiver Parameter für einen anhaltenden Therapieerfolg (sustained virological response, SVR) etabliert. Bei langsamem Abfall der Viruslast nach 12 bzw. 24 Wochen ist dagegen das Risiko für einen Relapse hoch. Eine individualisierte Therapiestrategie, die die jeweils vorhandenen prädiktiven Faktoren für jeden Patienten berücksichtigt, stellt ein wichtiges Ziel für die zukünftige Optimierung dieser nebenwirkungsreichen und kostenintensiven Therapie dar.1
Suche nach Polymorphismen
Abb.
1: SNP Microarray
Es wird schon lange vermutet, dass genetische Varianten (sogenannte „single nucleotide polymorphisms“ [SNPs] im Wirtsgenom) einen Einfluss auf den Verlauf und das Therapieansprechen einer HCV Infektion haben könnten. Für die Suche nach diesen genetischen Veränderungen gibt es verschiedene Möglichkeiten. In den letzten Jahren konnten die zugrundeliegenden genetischen Veränderungen zahlreicher Erkrankungen durch technische Weiterentwicklungen erkannt werden. Grundsätzlich gibt es die Möglichkeit, einen „Hypothesen-basierten“ und einen „Hypothesen-freien“ Analyse Ansatz zu verfolgen. In den meisten Fällen wird beim „Hypothesen-basierten“ Ansatz ein Kandidaten-Gen oder eine Kandidaten-Gen-Region, die für Proteine kodieren, die mit hoher Wahrscheinlichkeit pathophysiologisch für die Erkrankung relevant sind, genetisch untersucht. Sollten genetische Veränderungen identifiziert werden, untersucht man die Häufigkeit der Veränderungen in einem gesunden Kontrollkollektiv und kann somit eine genetische Assoziation bestätigen oder verwerfen.
Genomweite Assoziationsstudien (GWAS) hingegen folgen keiner biologisch plausiblen Hypothese. Diese Analyse Methode basiert auf der Tatsache, dass sich das menschliche Genom von fast jedem Individuum durch etwa 10 Millionen SNPs unterscheidet. Hierbei handelt es sich in den meisten Fällen um einen Basenaustausch der DNA, der funktionell keine Konsequenz hat. Beispielsweise führt der Basenaustausch nicht zu einer Veränderung der Proteinstruktur, da die kodierte Aminosäuresequenz gleich bleibt oder aber er liegt in nicht für ein Protein kodierenden Abschnitten. Dennoch stellen SNPs Marker des menschlichen Genoms dar und werden in Gruppen, sogenannten Haplotypen, vererbt. Durch die Vererbung in Gruppen ist es möglich, nur einen Teil der SNPs bei jedem Individuum zu untersuchen und Rückschlüsse auf die „gekoppelten“ SNPs innerhalb der jeweiligen Gruppe zu ziehen. Bei einer GWAS werden ohne eine definierte Hypothese in einem ausreichend großen Patientenkollektiv mit einer bestimmten Erkrankung bis zu einer Million (und mehr) solcher SNPs untersucht. Die Daten werden mit einem ethnisch ähnlichen, gesunden Kontrollkollektiv verglichen. So können genetische Unterschiede der SNPs in bestimmten Regionen der DNA erkannt werden. Anschließend kann in diesen Regionen ein für die Erkrankung verantwortliches Gen mit den entsprechenden Veränderungen oder in manchen Fällen auch direkt eine ursächliche genetische Veränderung identifiziert werden. Dies stellt einen wesentlichen Unterschied zum Kandidaten-Gen Ansatz dar, bei dem ein biologisch plausibles Gen direkt untersucht wird. Viele neue Studien in den unterschiedlichsten medizinischen Gebieten belegen, dass der genomweite Ansatz praktikabel und therapierelevant ist, da hierdurch komplexe genetische Assoziationen aufgedeckt werden können.
Bald auch in Leitlinien?
Zwar konnten in der Vergangenheit bereits einige SNPs insbesondere in Genen von Faktoren des angeborenen Immunsystems mit dem individuellen Verlauf einer HCV Infektion und der Therapieresponse assoziiert werden, diese wurden aber bisher nicht ernsthaft in die Therapieplanung einbezogen. Daher werden auch in den gerade aktualisierten Leitlinien zur Behandlung der HCV-Infektion praktisch ausschließlich virale Parameter (HCV Genotyp, initiale Viruslast und frühe Viruskinetik unter Therapie) in der Therapieplanung berücksichtigt.2
Dies dürfte sich in naher Zukunft ändern, nachdem weltweit mehrere Arbeitsgruppen praktisch zeitgleich und doch unabhängig voneinander mittels GWAS erstmalig Wirtsspezifische SNPs in der Region um das Interleukin 28B (IL28B) Gen identifizieren konnten, die eine äußerst robuste Assoziation sowohl mit dem sponta-nen Verlauf (selbst-limitierend oder chronisch) als auch mit den Erfolgsaussichten einer IFN-α basierten Kombinationstherapie (dauerhafte Viruselimination oder Nonresponse bzw. Relapse) bei der HCV Infektion aufweisen.3-6
IL28B kodiert Lambda-Interferone
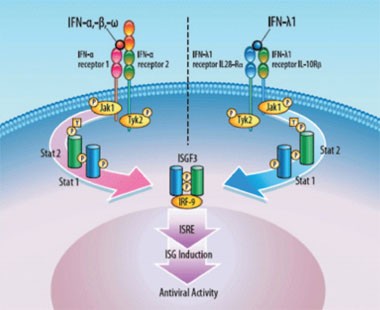
Abb.
2: Pegyliertes Interferon Lambda 1a
Die genomische Region um IL28B kodiert für Lambda Interferone (IFN-γ), die über einen eigenständigen Rezeptorkomplex eine potente IFN-α-ähnliche antivirale Immunantwort induzieren.7, 8 IFN-γ und IFN- α modulieren die angeborene antivirale Immunität über divergente wie auch synergistische Signalkaskaden.9 Neuere Studien konnten zudem bereits den erfolgreichen Einsatz von IFN-γ zur Inhibition der HCV Replikation in vitro10 und in ersten Phase 1B Therapiestudien zeigen (Shiffman et al.: PEG-IFN-lambda: antiviral activity and safety profile in a 4-week phase 1b study in relapsed genotype 1 hepatitis C infection. EASL 44th annual meeting April 2009 Copenhagen, Denmark [abstract 643]). Nach der aktuellen Datenlage könnten IFN-γ insbesondere auch aufgrund ihres im Vergleich zu IFN-α eher günstigen Nebenwirkungsprofils perspektivisch eine attraktive Alternative in der HCV Therapie darstellen.
Einfluss auf SVR
Die initialen GWAS konnten nun eindrucksvoll belegen, dass HCV-Genotyp-1 infizierte Patienten mit einem IL28B rs12979860 C-Allel oder einem IL28B rs8099917 T-Allel ein hoch-signifikant besseres Ansprechen auf eine pegIFN-α basierte Kombinationstherapie zeigen.3-5 Im Unterschied zu dem IL28B rs12979860 SNP scheint das IL28B rs8099917 Risiko G-Allel vor allem einen prädiktiven Marker für eine Nonresponse darzustellen.5 Zusätzlich beschrieben Tanaka et al. weitere Polymorphismen im IL28B Gen (z.B. IL28B rs12980275), die ebenfalls mit dem Therapie-Ansprechen bei chronischer HCV Genotyp-1 Infektion assoziiert werden konnten. Darüber hinaus konnte in zwei weiteren Studien gezeigt werden, dass Patienten mit einem IL28B rs12979860 C-Allel oder einem IL28B rs8099917 T-Allel auch eine deutlich höhere Chance auf eine spontane HCV Elimination nach akuter Infektion besitzen, was einen weiteren überzeugenden Hinweis für die funktionelle Relevanz dieser genetischen Variante darstellt.6, 11 Ein weiterer sehr spannender Befund war die Beobachtung, dass die Frequenz des IL28B rs12979860 Responder C-Allels in Abhängigkeit der Ethnizität deutliche Unterschiede zeigte, mit der niedrigsten Frequenz bei Afroamerikanern und der höchsten Frequenz bei Patienten asiatischer Herkunft. Somit könnte der seit langem bekannte Einfluss der Ethnizität auf die spontane Remissionsrate bzw. therapie-assoziierte SVR zu einem großen Teil auf der unterschiedlichen IL28B rs12979860 C-Allel Frequenz in den verschiedenen ethnischen Kohorten beruhen.3, 6 Zum ersten Mal ist damit ein Marker detektiert worden, der das schon lange bekannte Phänomen erklären kann, dass Afroamerikanier nach einer HCV Infektion seltener spontan das Virus eliminieren können bzw. schlechter auf die Therapie ansprechen als Europäer bzw. Asiaten.
Nicht nur bei GT1 wichtig
Nachdem die initialen IL28B Studien praktisch ausschließlich HCV Genotyp-1 (GT1) infizierte Patienten untersucht hatten, konnten wir jetzt in Kooperation mit dem Universitätsklinikum Frankfurt auch einen Einfluss des IL28B rs12979860 Responder C-Allels auf den Therapie-Verlauf bei Patienten mit einer HCV Genotyp 2/3 (GT2/3) Infektion belegen (Sarrazin C, Susser S, Doehring A, Lange C, Müller T, Herrmann E, Loetsch J, Zeuzem S, Berg T. Importance of IL28B gene polymorphisms in hepatitis C virus genotype 2 and 3 infected patients. J Hepatol 2010 in press). Die Non-response-Rate war bei T-Allel Trägern des IL28B rs12979860 SNPs mit 14% bzw. 21% (C/T bzw. TT Genotyp) signifikant höher als bei homozygoten C-Allel Trägern mit 3,5%. Auch Mangia und Kollegen konnten auf der diesjährigen EASL eine klare Assoziation des IL28B rs12979860 C-Genotyps mit einem Therapieerfolg bei Patienten mit HCV GT2/3 Infektion aufzeigen (Mangia et al.: Predictive role of IL28B C/C genotype on SVR and RVR in patients with genotype 2/3 chronic infection. EASL 45th annual meeting April 2009 Vienna, Austria [abstract 126]). Die Beobachtung, dass Patienten mit einer HCV GT2 Infektion überdurchschnittlich häufig homozygote IL28B rs12979860 C-Allelträger sind, ist ein interessanter Befund, der erstmals von McCarthy und Kollegen beschrieben worden war12 und auch in unserer aktuellen Kooperation mit Sarrazin und Kollegen belegt werden konnte. Demgegenüber scheinen sowohl der IL28B rs8099917 als auch der IL28B rs12980275 Polymorphismus keinen wesentlichen Einfluss auf den Therapie-Verlauf bei HCV GT2/3 infizierten Patienten auszuüben.11
Auch bei Patienten mit einer HCV/HIV Co-Infektion wird der Therapie-Verlauf von dem individuellen IL28B Genotypen des Patienten beeinflusst, wie erstmals von Rauch und Kollegen für den IL28B rs8099917 SNP gezeigt werden konnten. Rallón und Kollegen konnten jetzt auch für den IL28B rs12979860 SNP einen Einfluss auf die Therapie-assoziierte Ausheilung bei diesem in der Regel schwer behandelbaren Patientenkollektiv belegen.13
Keine Daten bei Tripletherapie
Es bleibt abzuwarten, welchen Effekt der IL28B Genotyp auf die Response einer HCV-Protease-Inhibitor-basierten Triple, oder einer IFN-γ−basierten Therapie besitzt. Erste Untersuchungen aus Japan bei Patienten mit einer Telaprevir-basierten Triple-Therapie sprechen jedoch auch in dieser Situation für ein deutlich besseres Therapie-Ansprechen bei den IL28B rs8099917 T/T und IL28B rs12979860 C/C Responder-Genotypen (Akuta N, Suzuki F, Hirakawa M, Kawamura Y, Yatsuji H, Se-zaki H, Suzuki Y, Hosaka T, Kobayashi M, Kobayashi M, Saitoh S, Arase Y, Ikeda K, Chayama K, Nakamura Y, Kumada H. Amino acid substitution in HCV core region and genetic variation near IL28 gene predict viral response to telaprevir with peginterferon and ribavirin. Hepatology 2010 in press). Somit scheint auch die Therapie-Erweiterung mit einem Proteaseninhibitor das Risiko eines Therapieversagens bei Patienten mit IL28B Risiko-Genotyp nicht gänzlich „ausgleichen“ zu können.
Aktuelle Daten EASL 2010
Allein während der diesjährigen EASL in Wien wurden 26 Beiträge mit Bezug zu IL28B und HCV in Form von Postern und Vorträgen akzeptiert. Diese Beiträge haben wir in Tabelle 1 kurz zusammengefasst. Trotz des enormen Wissenszuwachses bleiben die funktionellen Hintergründe der IL28B Varianten, die die etablierten „klassischen“ prädiktiven epidemiologischen und klinischen Wirtsfaktoren (Alter, Ge-schlecht, Ethnizität und Fibrosegrad) bezüglich ihrer Assoziation mit dem natürlichen und Therapie-induzierten Verlauf einer HCV Infektion bei weitem übertreffen bis dato unklar. So ist insbesondere die Interaktion zwischen IFN-γ und IFN-α bei der spontanen bzw. IFN-α-induzierten antiviralen Immunantwort nur bruchstückhaft verstanden. Es ist bekannt, dass periphere Monozyten von IL28B rs8099917 Risiko G-Allelträgern eine erniedrigte IL28B Transkription aufweisen4, 5, die auf eine reduzierte IFN-γ Aktivität bei diesen Patienten hinweisen könnte. Andererseits erscheint es paradox, dass sowohl bei HCV GT1-3, 12 als auch bei GT2/3-Infektion Patienten mit homozygotem IL28B rs12979860 C/C Responder-Genotyp eine signifikant höhere Baseline-Virämie zeigen, als die Patienten mit ungünstigem Response-Allel. Diese Assoziation von günstigem Response-Allel mit hoher Viruslast könnte Ausdruck einer geringeren endogenen bzw. spontanen Immunantwort sein. Die niedrige intrahepatische Expression sogenannter „Interferon-stimulierbarer Gene“ (ISG) bei homozygoten IL28B rs8099917 Responder T-Allel Trägern passt in das Konzept einer herabgesetzten endogene angeborene antivirale Immunität bei diesen Patienten.14 Es konnte bereits früher gezeigt werden, dass unbehandelte Patienten mit niedriger intraheptischer ISG Expression im Gegensatz zu Patienten mit bereits initial maximal aktivierten ISG besser auf eine exogene Stimulation mit IFN-α ansprechen und daher unter der Therapie auch häufiger eine dauerhafte Viruselimination erreichen. Dies scheint sich somit auch bei Patienten mit einem homozygoten IL28B rs12979860 C/C Responder-Genotyp zu bestätigen.
| Abstract # | Zusammenfassung der wesentlichen Beobachtungen |
|---|---|
| # 3 Thompson et al. | Eine
reduzierte intrahepatische ISG Expression bei Patienten mit IL28B
rs12979860 C/C Genotyp prädisponiert für potente Immunanwort nach exogener IFN Therapie |
| # 76 Bignulin et al. | Der
IL28B rs12979860 T-Allelstatus korreliert mit dem Risiko einer
Virus-assoziier- ten Leberzirrhose und Entwicklung eines HCC |
| #
125 Tillmann et al. | Der IL28B rs12979860 Genotyp
korreliert mit dem Auftreten eines Ikterus und spontaner Viruselimination bei akuter HCV Infektion in der deutschen Anti-D Kohorte |
| #
126 Mangia et al. | Der IL28B rs12979860 Genotyp
beeinflusst RVR und SVR Raten bei Patienten mit HCV GT2/3 Infektion. Die RVR ist unabhängig vom IL28B Genotyp ein starker Prä- diktor für SVR |
| # 297 Rutter et al. | Eine Silibilin Monotherapie reduziert auch bei
ehemaligen Nonrespondern mit einem IL28B rs12979860 Risiko T-Allel effektiv die Viruslast, was auf einen von IFN unterschiedlichen Wirkmechanismus von Silibinin hindeutet |
| # 657 Maekawa et al. | IL28B rs8099917 Risiko G-Allel Träger zeigen eine
abgeschwächte frühe Viruskine- tik unter Therapie (keine RVR bei 170 Patienten) |
| # 1165 Eurich et al. | Der IL28B rs8099917 Genotyp korreliert mit
Entzündungszeichen in Lebertrans- plantaten in den ersten drei Jahren nach Transplantation |
# 1166 Fried et al. | Die Kombination von IL28B rs12979860 Genotyp und
Serumwert des Interferon-? induzierbaren Proteins-10 (IP-10) verbessert die Vorhersagbarkeit eines Therapie- erfolges (SVR vs. Nonresponse) |
# 1167 Halfon et al. | Der IL28B rs8099917 Genotyp korreliert auch in
einer französischen Kohorte mit dem Therapieansprechen auf Kombinationstherapie |
# 1168 Howell et al. | Der IL28B rs12979860 Genotyp korreliert mit der
frühen Viruskinetik innerhalb der ersten 28 Tage nach Therapiebeginn bei Patienten mit HCV GT1 Infektion |
| # 1169 Kurosaki et al. | Weitere Bestätigung des IL28B rs8099917
G-Allelstatus als Prädiktor für Nonres- ponse auf Kombinationstherapie |
| # 1170 Mangia et al. | Bestätigung der Assoziation des IL28B rs12979860 C-Allels mit
einer spontanen HCV Elimination bei Patienten mit Thalassemia major |
| #
1171 Matsuura et al. | Bestätigung der Assoziation des IL28B rs8099917
T-Allels mit einer spontanen HCV Elimination bzw. Assoziation des IL28B rs8099917 G-Allels mit einer Persistenz der HCV Infektion bei japanischen Patienten |
| # 1172 Nischalke et al. | Limitierter Einfluss des IL28B rs12979860
Genotyps auf den Therapieerfolg bei Patienten mit HCV/HIV Co-Infektion |
| # 1173 Neukam et al. | Der IL28B rs12979860 C/C Genotyp ist ein positiver
Prädiktor für einen Therapie- erfolg bei Patienten mit HCV/HIV Co-Infektion |
| # 1174 O’Brien et al. | Der IL28B rs12979860 Genotyp beeinflusst auch
bei Patienten mit fortgeschritte- ner HCV-assoziierter Lebererkrankung aus dem HALT-C Trial den Erfolg einer Kom- binationstherapie |
| #
1175 Romero-Gómez et al. | Überrepräsentation des IL28B rs12979860 C/C Genotyps bei
Patienten, die nicht mit HCV GT 1 infiziert sind. Bestätigung der Assoziation des IL28B rs12979860 C/C Genotyps mit spontaner HCV Elimination. Assoziation des IL28B rs12979860 C/C Genotyps mit Therapie-Ansprechen nur bei HCV GT1 |
| # 1176 Trippler et al. | Spärliche Expression von Typ III-IFN (IL28a,
IL28b, Il29) in Leberbiopsien von Pati- enten mit chronischer HCV Infektion spricht gegen einen exponierten Einfluss der γ-IFN auf hepatische ISGs |
| # 1177 Stättermayer et al | Das IL28B rs12979860 Risiko T-Allel ist ein
negativer Prädiktor für das Therapiean- sprechen bei HCV GT1, aber nicht bei HCV GT 2/3. Unterschiedliche Prävalenzen des C/C-Genotyps bei HCV GT1, 2/3 und 4 |
| # 1178 Tanaka et al. | Der IL28B rs8099917 G-Allelstatus ist der
wichtigste Prädiktor für Nonresponse auf Kombinationstherapie. Reduzierte IL28A/B Transkription in peripheren Blutzellen bei Patienten mit einem IL28B rs8099917 G-Allel |
| # 1179 Li et al. | Der IL28B rs12979860 C/C Genotyp korreliert mit
erhöhten LDL-Cholesterin Spie- gel bei Patienten mit chronischer HCV Infektion. Dies wird vor dem Hintergrund der bekannten Interaktion zw. IFN und dem LDL-Metabolismus als abgeschwächte endogene IFN-Immunantwort bei diesen Patienten gedeutet |
| #
1180 Asselah et al. | Der IL28B rs12979860 Genotyp beeinflusst den
Therapieerfolg auch bei einer Monotherapie mit pegIFN oder einer Kombinationstherapie mit nicht-pegyliertem IFN und Ribavirin |
| #
1181 McHutchison et al. | Die therapeutische Vakzine GI-5005 optimiert
die frühe Viruskinetik unabhängig vom IL28B rs12979860 Genotyp und zeigt den stärksten Effekt bei Patienten mit IL28B rs12979860 T/T Risiko-Genotyp |
| # 1182 Par et al. | Bestätigung der Assoziation des IL28B rs12979860 C/C
Genotyps mit spontaner HCV Elimination sowie Therapie-Erfolg bei ungarischen Patienten mit HCV GT1 |
| # 1187 Dill et al. | IL28B Risiko-Genotypen sind mit erhöhter intrahepatischer
ISG Expression und erniedrigter IL28B Expression assoziiert. Die ISG Expression war hierbei unabhän- gig vom IL28B Genotyp und ein besserer prädiktiver Parameter für das Therapie- Ansprechen |
| #
2011 Neumann et al. | IL28B rs12979860 C/C Genotypen zeigen höhere RVR
Raten. IL28B Genotyp-asso- ziierte Unterschiede in der frühen Viruskinetik zeigen sich besonders nach 24h bzw. in der ersten Phase der IFN-induzierten Viruselimination. Ein ähnlicher Trend wird auch für nicht HCV GT1-infizierte Patienten postuliert, die erneut eine unterschied- liche Verteilung der IL28B Genotypen aufwiesen |
Tab. 1: Aktuelle Beiträge zum Thema IL28B und HCV während der EASL 2010
Wirkmechanismus
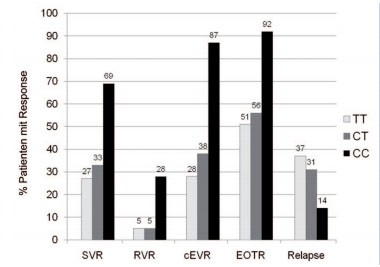
Abb. 1: Bedeutung des IL28B
rs12979860 Genotyps (CC, CT und TT) auf die Peg-IFNα plus
Ribavirin-induzierte Therapie-Response bei kaukasischen Patienten mit HCV-Typ
1-Infektion. (SVR=anhaltende Remission; RVR=rasche virologische Response zur
Woche 4; cEVR=komplette virologische Response zur Woche 12; EOTR=komplette
Response am Therapieende; Relapse=Rückfall nach Therapieende bei Patienten mit
kompletter virologischer Response unter Therapie). Modifiziert nach Thompson AJ
et al.15
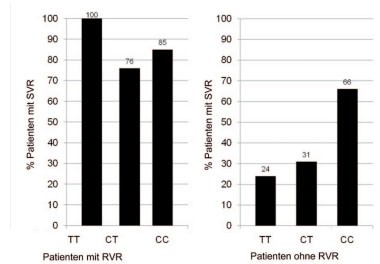
Abb. 2: Bedeutung des IL28B
rs12979860 Genotyps (CC, CT und TT) auf die Peg-IFNα plus
Ribavirin-induzierte SVR Rate in Abhängigkeit von der frühen Response zur Woche
4 (=RVR) bei kaukasischen Patienten mit HCV-Typ 1-Infektion (SVR=anhaltende
Remission). Modifiziert nach Thompson AJ et al.15
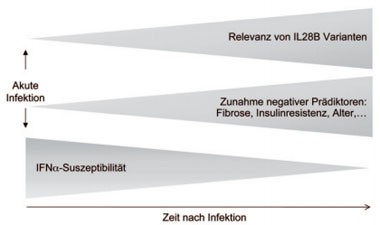
Abb. 3: Relative Bedeutung des IL28B Genotyps für die IFNα -Suszeptibilität in Abhängigkeit vom Stadium der HCV
Infektion. Patienten mit akuter HCV-Infektion besitzen unabhängig vom Virus-Typ
oder Wirtsgenetischen Faktoren eine hohe Interferon-Suszeptibilität, d.h.
praktisch alle Patienten sprechen in diesem Stadium auf eine IFNα -Therapie an. Mit zunehmender Dauer der Infektion und
Akquirieren zusätzlicher negativer Responsefaktoren gewinnt der genetische IL28B Risikofaktor an Bedeutung
Der signifikante Effekt des IL28B Genotyps auf die Suszeptibilität der IFN-α Response lässt sich eindeutig anhand der frühen viralen Kinetik unter Therapie ablesen. Patienten mit einem IL28B rs12979860 C/C Responder-Genotyp zeigen einen rascheren Abfall der Viruslast und erreichen damit deutlich häufiger eine RVR als Patienten mit dem Nonresponder T-Allel (Abb. 1). Die gesteigerte RVR Rate stellt einen wesentlichen Faktor für die beobachtete höhere SVR Rate dar. Interessant sind die Befunde, dass jedoch besonders bei Patienten ohne RVR der Einfluss der Il28B Genotypen deutlich wird, während bei RVR der Einfluss des IL28B Genotyps auf die SVR verloren geht (Abb. 1 und 2).15
Nach einer neuen Studie von Li und Kollegen könnte auch ein Einfluss des IL28B Polymorphismus auf den endogenen Cholesterol-Metabolismus, der nach unserem bisherigen Kenntnisstand eng mit dem HCV Lebenszyklus assoziiert ist, eine Rolle spielen.16 Während wir zunehmend verstehen, warum Patienten mit einem günstigen IL28B Genotypen trotz möglicherweise herabgesetzter endogener antiviraler Aktivität besser auf eine exogene antivirale Therapie mit Interferon ansprechen, bleibt es letztlich weiterhin unklar, warum diese Patienten auch eine erhöhte spontane HCV Eliminationsrate aufzuweisen scheinen.
Konsequenzen für die Praxis
In der Zusammenschau der uns aktuell vorliegenden Daten ist es sehr wahrscheinlich, dass in Zukunft die individuelle IL28B Genotypisierung als prädiktiver genetischer Parameter einen substantiellen Einfluss auf die Risikostratifizierung und den Therapie-Algorithmus sowohl bei Patienten mit akuter als auch chronischer HCV Infektion haben wird. Die IL28B Genotypisierung ist im klinischen Alltag praktikabel, weil sie im Gegensatz zur ISG Bestimmung mittels Leberbiopsie, einfach anhand einer Blutprobe mittels etablierter PCR-basierter Testverfahren durchgeführt und im Gegensatz zur frühen Viruskinetik bereits vor Therapiebeginn mit in die therapeutischen Entscheidungsprozesse einbezogen werden kann. Ebenso bietet die individuelle IL28B Genotypisierung die Möglichkeit, noch unentschlossene Patienten mit einem günstigen IL28B Genotyp zu einer Therapie zu motivieren oder die allgemeine Therapie-Adhärenz zu erhöhen. Im Umkehrschluss sollte trotz der allgemeinen Euphorie über die zunehmende Personalisierung der HCV Therapie bedacht werden, dass auch fast jeder dritte Patient mit einem IL28B rs12979860 T/T Risiko-Genotyp eine SVR erreichen kann.3 Somit sollte die IL28B Genotypisierung nicht dazu verwendet werden, einem Patienten mit einer IL28B Risikokonstellation von vornherein von einer möglichen Therapie abzuraten. Daher werden in der nun anbrechenden IL28B Ära in der täglichen klinischen Praxis weiterhin die etablierten virus- und wirtspezifischen prädiktiven Parameter und insbesondere auch die frühe Viruskinetik unter Therapie mit in die Therapieplanung und Risikostratifizierung einbezogen werden müssen (Abb. 3). Neue Studien zur Therapiedauer und -dosierung der IFN-α basierten Kombinationstherapie in Abhängigkeit des individuellen IL28B Genotyps werden sicherlich in absehbarer Zeit folgen. Ebenso erscheint es konsequent, dass die IL28B Genotypisierung bei allen zukünftigen HCV-assoziierten Studien mit in die Stratifizierung einbezogen werden sollte. Wir sehen somit sehr spannenden Zeiten entgegen und es ist schon jetzt absehbar, dass die Kenntnis des individuellen IL28B Genotyps unser Bestreben, jedem Patienten mit Hepatitis C eine personalisierte Therapie unter Maximierung des Therapieerfolgs und Minimierung vermeidbaren Therapieversagens zukommen zu lassen, einen großen Schritt voranbringen wird.
1 Berg T. Tailored treatment for hepatitis C. Clin Liver Dis 2008;12:507-528, vii-viii.
2 Sarrazin C, Berg T, Ross RS, Schirmacher P, Wedemeyer H, Neumann U, Schmidt HH, et al. [Prophylaxis, diagnosis and therapy of hepatitis C virus (HCV) infection: the German guidelines on the management of HCV infection]. Z Gastroenterol;48:289-351.
3 Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, Heinzen EL, et al. Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance. Nature 2009;461:399-401.
4 Suppiah V, Moldovan M, Ahlenstiel G, Berg T, Weltman M, Abate ML, Bas-sendine M, et al. IL28B is associated with response to chronic hepatitis C in-terferon-alpha and ribavirin therapy. Nat Genet 2009;41:1100-1104.
5 Tanaka Y, Nishida N, Sugiyama M, Kurosaki M, Matsuura K, Sakamoto N, Nakagawa M, et al. Genome-wide association of IL28B with response to pegy-lated interferon-alpha and ribavirin therapy for chronic hepatitis C. Nat Genet 2009;41:1105-1109.
6 Thomas DL, Thio CL, Martin MP, Qi Y, Ge D, O‘Huigin C, Kidd J, et al. Ge-netic variation in IL28B and spontaneous clearance of hepatitis C virus. Nature 2009;461:798-801.
7 Kotenko SV, Gallagher G, Baurin VV, Lewis-Antes A,
Shen M, Shah NK, Langer JA, et al. IFN-lambdas mediate antiviral protection through a distinct class II cytokine receptor complex. Nat Immunol 2003;4:69-77.
8 O‘Brien TR. Interferon-alfa, interferon-lambda and hepatitis C. Nat Genet 2009;41:1048-1050.
9 Marcello T, Grakoui A, Barba-Spaeth G, Machlin ES, Kotenko SV, MacDonald MR, Rice CM. Interferons alpha and lambda inhibit hepatitis C virus replication with distinct signal transduction and gene regulation kinetics. Gastroenterology 2006;131:1887-1898.
10 Robek MD, Boyd BS, Chisari FV. Lambda interferon inhibits hepatitis B and C virus replication. J Virol 2005;79:3851-3854.
11 Rauch A, Kutalik Z, Descombes P, Cai T, Di Iulio J, Mueller T, Bochud M, et al. Genetic variation in IL28B is associated with chronic hepatitis C and treat-ment failure: a genome-wide association study. Gastroenterology;138:1338-1345, 1345 e1331-1337.
12 McCarthy JJ, Li JH, Thompson A, Suchindran S, Lao XQ, Patel K, Tillmann HL, et al. Replicated Association Between an Interleukin-28B Gene Variant and a Sustained Response to Pegylated Interferon and Ribavirin. Gastroen-terology.
13 Rallon NI, Naggie S, Benito JM, Medrano J, Restrepo C, Goldstein D, Shianna KV, et al. Association of a single nucleotide polymorphism near the interleukin-28B gene with response to hepatitis C therapy in HIV/hepatitis C virus-coinfected patients. AIDS;24:F23-29.
14 Honda M, Sakai A, Yamashita T, Nakamoto Y, Mizukoshi E, Sakai Y, Naka-mura M, et al. Hepatic ISG expression is associated with genetic variation in IL28B and the outcome of IFN therapy for chronic hepatitis C. Gastroenterol-ogy.
15 Thompson AJ, Muir AJ, Sulkowski MS, Ge D, Fellay J, Shianna KV, Urban T, et al. IL28B Polymorphism Improves Viral Kinetics and Is the Strongest Pre-treatment Predictor of SVR in HCV-1 Patients. Gastroenterology.
16 Li JH, Qian Lao X, Tillmann HL, Rowell J, Patel K, Thompson A, Suchindran S, et al. Interferon-lambda genotype and low serum low-density lipoprotein cholesterol levels in patients with chronic hepatitis C infection. Hepatology.





