Die Sicherheit und Wirksamkeit von G/P bei Patienten mit Drogengebrauch II
Hintergrund und Zielsetzung
Die pangenotypische HCV-Kombinationstherapie aus Glecaprevir (Protease-Inhibitor) und Pibrentasvir (NS5AInhibitor) hat in Phase-2- und Phase-3-Studien hohe Heilungsraten sowie eine gute Verträglichkeit beim HCV Genotyp 3 gezeigt.
Methodik
In der vorliegenden Analyse wurden die Heilungsraten und Sicherheitsdaten aller therapienaiven Genotyp 3 Patienten mit und ohne kompensierter Zirrhose, die im AbbVie Phase-2/3-Studienprogramm eine 8- oder 12-wöchige Glecaprevir/Pibrentasvir (G/P) Therapie erhalten hatten, gepoolt. Primärer Endpunkt war das anhaltende Therapieansprechen 12 Wochen nach Therapieende (SVR12). Sicherheitsdaten (Nebenwirkungen, Laborwertveränderungen) wurden ebenfalls ausgewertet.
Ergebnisse
Abbildung: SVR12 by Intent-to-treat (ITT) and modified ITT (mITT)
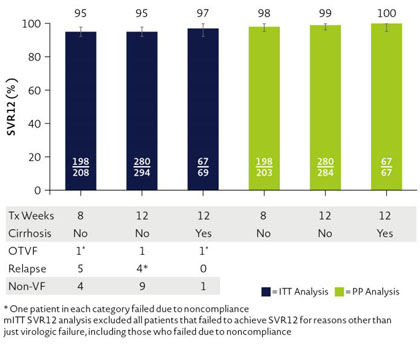
Insgesamt wurden 571 Genotyp-3-Patienten behandelt. Hierunter waren 208 bzw. 294 Patienten ohne Zirrhose, die eine 8- bzw. 12-wöchige Therapie erhalten hatten; 69 Patienten mit Zirrhose wurden für 12 Wochen behandelt. Insgesamt 22 % der Patienten hatten Baseline-Resistenzen im NS5A-Gen (Positionen 24, 28, 30, 31, 58, 92, 93), 17 % hatten eine gleichzeitige Opiatsubstitutionstherapie erhalten. In der ITT-Analyse erreichten 95 % (n=198/208) der Patienten ohne Zirrhose nach 8-wöchiger Therapie und ebenfalls 95 % (n=280/294) nach 12-wöchiger Therapie einen SVR12. In der modifizierten ITT-Analyse (ohne nicht-virologische Versager) lagen die SVR12-Raten bei 98 % (n=198/203) bzw. 99 % (n=280/284). Insgesamt erlitten 9 Patienten einen Relapse (5 nach 8-wöchiger Therapie und 4 nach 12-wöchiger Therapie). Patienten mit der NS5A-RAS A30K hatten nach 8-wöchiger Therapie (SVR12: 84 %; n=16/19) numerisch ein etwas schlechteres Therapieansprechen als nach 12-wöchiger Therapie (SVR12: 94 %; n=17/18), allerdings war dieser Unterschied nicht statistisch signifikant. Die SVR12-Raten der Patienten mit Zirrhose lagen bei 97 % (n=67/69) in der ITT-Analyse und 100 % (n=67/67) in der mITT-Analyse. Nebenwirkungen, die bei 10 % der Patienten oder mehr mehr auftraten waren Kopfschmerzen, Fatigue und Übelkeit. Schwere medikamenten-assoziierte Nebenwirkungen oder Grad-3-Leberwerterhöhungen traten nicht auf.
Fazit
Die G/P Kombination wurde insgesamt sehr gut vertragen und erzielte hohe SVR12-Raten bei therapienaiven Patienten mit Genotyp 3. Eine Therapiever-längerung auf 12 Wochen ist für Patienten ohne Zirrhose nicht angezeigt.
 PD Dr. med. Johannes Vermehren
PD Dr. med. Johannes Vermehren
Oberarzt der Medizinischen Klinik I,
Universitätsklinikum Frankfurt,
Theodor-Stern-Kai 7,
60590 Frankfurt am Main
Kommentar PD Dr. med. Johannes Vermehren
Seit Einführung der direkt antiviralen Substanzen steht der HCV Genotyp 3 im Fokus der Aufmerksamkeit, da die ersten Interferon-freien Kombinationen (Sofosbuvir und Ribavirin für 24 Wochen bzw. Daclatasvir und Sofosbuvir für 12-24 Wochen) insbesondere bei Patienten mit Zirrhose deutlich geringere Ansprechraten aufwiesen. Mit VEL/SOF steht seit Sommer 2016 eine 12-wöchige Therapie für Genotyp-3-Patienten zur Verfügung, die in Studien hohe Ansprechraten aufweisen konnte (Foster et al. NEJM 2015; Curry et al. NEJM 2015). Mit G/P besteht nun eine weitere Therapieoption, die bei unbehandelten Patienten ohne Zirrhose sogar auf 8 Wochen verkürzt werden kann. Ein zusätzlicher Nutzen dieser Therapie liegt darin, dass G/P auch bei Patienten mit fortgeschrittener bzw. terminaler Niereninsuffizienz eingesetzt werden kann. Ein wichtiger Aspekt, den die vorliegende Analyse zu beantworten hatte, ist die Bedeutung der Baseline-Resistenzen für diese Kombination. Interessanterweise zeigte sich, dass bei vorliegender Y93H-Variante alle Patienten, die eine 8-wöchige Therapie erhalten hatten, geheilt wurden, wohingegen 2/20 Patienten nach 12-wöchiger Therapie einen Relapse erlitten. Für die A30K-Substitution fanden sich numerisch mehr Relapser nach 8 als nach 12 Wochen (n=3/19 vs. n=1/18). Der Unterschied war statistisch nicht signifikant, sollte meines Erachtens aber in Real-World-Kohorten anhand größerer Patientenzahlen weiter untersucht werden.
 Prof. Dr. med.
Prof. Dr. med.
Wolf-Peter Hofmann
Gastroenterologie am
Bayrischen Platz,
Innsbrucker Str. 58,
D-10825 Berlin
Kommentar Prof Dr. med. Wolf-Peter Hofmann
Die Behandlung des HCV-Genotyps 3 hat seit Beginn der DAA-Ära immer wieder für Überraschungen gesorgt. Aus dem einst „easy to treat“ Genotyp 3 wurde der HCV-Problem-Genotyp mit niedrigeren Ansprechraten im Vergleich zum Genotyp 1. Das G/P Entwicklungsprogramm von der Firma AbbVie hat sämtliche HCV-Subgruppen bedacht und in der vorliegenden Studie wurde nun eine Analyse von insgesamt 571 HCV-Genotyp-3-Patienten als sog. gepoolte Datenpräsentation vorgelegt. Die einfache Botschaft, dass nicht-zirrhotische, therapieunerfahrene Patienten für 8 Wochen behandelt werden können, wird überzeugend untermauert. Bei den therapieunerfahrenen Patienten mit bereits etablierter Zirrhose ist eine 12-wöchige Therapie mit exzellenten SVR-Raten vergesellschaftet. Das Nukleosidanalogon Ribavirin wird bei dem G/P-Regime nicht benötigt. Aufgrund des enthaltenen HCV-NS3-Proteasehemmers Glecaprevir steht G/P nicht für Patienten mit fortgeschrittener, dekompensierter Leberzirrhose zur Verfügung. Therapieerfahrene Patienten mit HCV Genotyp 3 sollten laut Fachinformation weiterhin eine Therapie für 16 Wochen erhalten.





