DR. FRANK TACKE UND PROF. CHRISTIAN TRAUTWEIN, AACHEN
 Hepatitis B
Impfung:
Hepatitis B
Impfung:
Unzureichender Schutz vor Infektion mit seltenen Genotypen
Gemäß der WHO-Empfehlung werden Kinder, Jugendliche und Personen mit Risikokontakten in Deutschland gegen das Hepatitis B Virus (HBV) geimpft. Wir berichten über einen immunkompetenten erwachsenen Patienten, der trotz Impfung eine akute HBV-Infektion erworben hat. Möglicherweise vermitteln die aktuell verfügbaren Impfstoffe keinen vollständigen Schutz vor Infektionen mit seltenen HBV-Genotypen.
In unserer Sprechstunde stellte sich ein 32jähriger Patient mit den typischen Symptomen einer akuten Virushepatitis (Abgeschlagenheit, Ikterus, generalisiertes Exanthem, Transaminasenerhöhung von ALT 567 U/L und AST 525 U/L) vor4. In der serologischen Diagnostik zeigten sich die typischen Befunde einer akuten HBV-Infektion, nämlich Nachweis von HBsAg, HBeAg, anti-HBc IgM und 26.700 Kopien/ml HBV-DNA. Der Patient hatte keine relevanten Vorerkrankungen, war vollkommen immunkompetent und wurde negativ für andere hepatotrope Viren oder Autoantikörper getestet. Interessanterweise hatte der Patient 10 Monate vor Auftreten der Symptome der akuten HBV-Infektion eine Twinrix®-Impfung gemäß der allgemeinen Empfehlungen beendet. Seine anti-HBs-Titer lagen in zwei unabhängigen Testsystemen mit 50 IU/L (Abbott) bzw. 82 IU/L (Dade Behring) im sogenannten "protektiven" Bereich3. Die akute Infektion wurde entsprechend der Leitlinien ausschließlich symptomatisch behandelt1 und heilte im Verlauf von 6 Monaten mit HBs- und HBe-Serokonversion vollständig aus. Wie HBV übertragen worden war, ließ sich nicht eruieren. Der Patient verneinte typische Risikofaktoren oder Verhaltensweisen, war aber bis zwei Wochen vor Beginn der Symptome für mehrere Wochen als Bergbauingenieur in Spanien tätig gewesen.
INFEKTION TROTZ "PROTEKTIVER" TITER
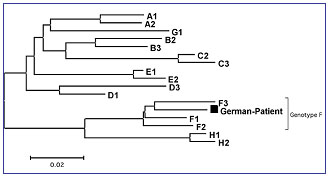
Abb. 1: Stammbaumrekonstruktion (‚phylogenetic tree’) für die genetische Sequenz der
HBV-Variante des beschriebenen Patienten (‚German Patient’) im Vergleich zu Konsensus-Sequenzen
für die bekannten HBV-Geno- typen A-H. Der Patient war demnach mit HBV des Genotyps F infiziert. Die
Skala zeigt die prozentuale Nukleotid-Divergenz an.
Das Auftreten einer HBV-Infektion trotz ‚protektiver' anti-HBs-Titer (>10 U/l) ist nur in Einzelfällen beschrieben. Fast ausschließlich handelte es sich dabei um eine HBV-Reaktivierung bei immunsupprimierten Patienten, z.B. nach Chemotherapie oder bei AIDS-Erkrankung4. Daher haben wir die virale DNA aus dem Serum dieses immunkompetenten Patienten isoliert und sequenziert. Eine phylogenetische Analyse der Sequenz ergab, dass der Patient mit HBV des Genotyps F infiziert war (Abb. 1) - ein Genotyp, der vor allem in Süd- und Mittelamerika (Tab. 2) vorkommt und bislang in Westeuropa noch nicht beschrieben worden ist5. Besondere Mutationen im Bereich des Hüllproteins (HBsAg) oder des bekannten Epitops (‚a-determinant region'), die spezifisch eine verminderte Antikörper-Bindung erklären könnten, fanden sich hingegen nicht6.
| Aktive Schutzimpfung rekombinantes HBsAg (Hüllprotein) | u.a. Engerix-B® (GlaxoSmithKline), HBVAXPRO® (Aventis Pasteur MSD); Twinrix® (Glaxo, Hep.A+B); Infanrix hexa® (Glaxo, DPT+Polio+Hib+Hep.B) |
| Indikation | alle Neugeborenen und Kinder beruflich Exponierte (s.Text) Risikogruppen (s.Text) Patienten mit chronischen Lebererkrankungen Patienten mit progredienten chron. Nierenerkrankungen |
| Grundimmunisierung | Erstimpfung (Monat 0) + nach 1 + nach 6 Monaten |
| Auffrischimpfung | nach anti-HBs Titer (4-8 Wochen nach Grundimmunis.) <10 IU/ml: sofort und erneute Kontrolle* 10-100 IU/ml: innerhalb eines Jahres und Kontrolle >100 IU/ml: Auffrischimpfung nach 10 Jahren |
| Kontraindikation | Allergie gegen Impfstoffkomponente (selten) keine Impfung, wenn HBsAg positiv (= HBV-Infektion) |
| Nebenwirkungen | Lokale Reaktionen (Rötung, Schwellung, Schmerz, Verhärtung), selten Allgemeinreaktionen (Fieber, Kopfschmerzen, Krankheits- gefühl); bislang kein Nachweis von Assoziation mit Autoimmun- erkrankungen oder ALL |
| Kosten | ca. 150-180 für 3 Impfdosen (Erwachsene) |
| * Geimpfte mit anti-HBs <10 IU/ml 4-8 Wochen nach Grundimmunisierung gelten als Non-Responder und sollten sofort nach- geimpft und 4 Wochen später kontrolliert werden. Insgesamt sind bis zu drei zusätzliche Impfungen in 1-3 Monaten, evtl. in doppelter Dosis („Dialysedosis“), sinnvoll. | |
HBV-GENOTYPEN
| Genotyp | Hauptsächliches Auftreten |
|---|---|
| A | Europa (Nordeuropa), Afrika, Indien, USA |
| B | Asien, USA |
| C | Asien, USA |
| D | Europa (Südeuropa), USA, Indien, Mittlerer Osten |
| E | Afrika (West/Süd) |
| F | Südamerika, Mittelamerika |
| G | Europa, USA |
| H | Südamerika, Mittelamerika, USA |
Tab. 2: Geographische Verteilung der HBV Genotypen
Derzeit unterscheidet man acht verschiedene HBV-Genotypen (A-H), die sich in mindestens 8% der Nukleotidsequenzen unterscheiden. Diese Genotypen zeigen ein unterschiedliches geographisches Verteilungsmuster: In Deutschland und Nord-/ Westeuropa ist der Genotyp A dominierend, während in Asien die Genotypen B und C und im Mittelmeerraum der Genotyp D vorherrschen (Tab. 2). Unser Verständnis der möglichen klinischen Bedeutung der HBV-Genotypen ist noch unvollständig - doch die Genotypen scheinen z.T. deutliche Unterschiede im klinischen Verlauf, im Ansprechen auf Therapien wie Interferonbehandlung oder in der Häufigkeit der Entwicklung eines hepatozellulären Karzinoms zu zeigen5. Der Genotyp F scheint fast ausschließlich in Mittel- und Südamerika aufzutreten und zeigt eine große Sequenzabweichung besonders von den in der westlichen Welt führenden Genotypen A und D (vgl. Abb. 1).
IMPFSTOFF GEGEN A UND D
Wer soll geimpft werden?
Aufgrund der potentiell lebensbedrohlichen Komplikationen der chronischen HBV-Infektion und Schwierigkeiten in der Therapie kommt der Prävention der HBV-Infektion oberste Priorität zu. Daher wird von der WHO die aktive Schutzimpfung gegen HBV für alle Neugeborenen und alle Nichtgeimpften vor Erreichen der Pubertät empfohlen3. Die ständige Impfkommission am Robert Koch-Institut (STIKO) empfiehlt die Aktivimpfung für Säuglinge ab dem 3. Lebensmonat und Kinder sowie alle Personengruppen mit erhöhtem Risiko (d.h. Personal im Gesundheitswesen/Fürsorgeeinrichtungen, Empfänger von Blut/Plasmaprodukten, Drogenabhängige, Homosexuelle, Reisende in Endemiegebiete, Angehörige HBsAg-positiver Patienten, Dialysepatienten). Patienten mit chronischen Lebererkrankungen, die anti-HBc negativ sind, sollten ebenfalls immunisiert werden. Da das Virus sehr infektiös ist und neben Blut, perinatal oder sexuell auch durch engen Kontakt übertragen werden kann, sollte die Impfindikation im Zweifelsfall großzügig gestellt werden und z.B. auch durch Kontakt mit HBsAg Trägern gefährdete Personen im Haushalt oder in einer Gemeinschaft (z.B. Kindergärten, Schulklassen, Pflegestätten) einschließen. Wichtig ist ebenfalls, dass alle im medizinischen Bereich tätigen Personen (inkl. Helferinnen, Studierende, Reinigungspersonal) vor Aufnahme ihrer Tätigkeit einen vollständigen Impfschutz aufweisen1.
In der aktiven Immunisierung werden rekombinante Proteine der Genotypen A bzw. A und D eingesetzt3, so z.B. HBsAg des Genotyps A im Impfstoff Twinrix®7. Vergleicht man die Sequenzen der HBV-Genotypen, so finden sich allein im immunogenen Epitop des Hüllproteins (‚a-determinant region') vier ausgetauschte Aminosäuren zwischen Genotyp F und A bzw. D4. Zumindest einzelne dieser Veränderungen können in vitro eine verminderte Bindung der anti-HBs Antikörper an das virale Protein bewirken8. Daher ist es denkbar, dass aufgrund dieser Sequenzunterschiede die in Deutschland gegen die Genotypen A und D entwickelten Impfstoffe gegen hierzulande seltene Genotypen nicht ausreichend schützen - wie in dem beschriebenen Fall des deutschen Patienten, der sich trotz Impfung mit HBV-Gentoyp F infizierte. Zukünftige HBV-Impfstoffe sollten daher möglicherweise, auch angesichts zunehmender weltweiter Reise- und Migrationsbewegungen, immunodominante Proteine verschiedener Genotypen enthalten.
PRAKTISCHES VORGEHEN
Die heute in Deutschland gängigen Impfstoffe (Tab. 1) enthalten rekombinant hergestellte HBsAg-Partikel (small HBsAg = virales Hüllprotein) sowie Aluminiumhydroxid als Adjuvanz. Neben den Einzelimpfstoffen gibt es auch Kombinationspräparate, z.B. für die kombinierte Hepatitis-A- und -B-Impfung (z.B. Twinrix®). Die Grundimmunisierung besteht aus drei intramuskulären Injektionen zum Zeitpunkt 0, nach 1 und nach 6 Monaten. Der Erfolg der Immunisierung kann durch Kontrolle der anti-HBs Titer überprüft werden. Bei Impflingen, die keiner spezifischen Risikogruppe angehören, gesund und jünger als 40 Jahre sind (d.h. im allgemeinen gesunde Kinder und Jugendliche nach der Grundimmunisierung), ist eine Testung nach derzeitigem Konsens nicht notwendig1; bei allen übrigen sollte der Impferfolg kontrolliert werden. Wird durch die Impfung ein anti-HBs Titer >100 IU/ml erreicht, ist von einem Schutz für mindestens 10 Jahre auszugehen, bei Titern zwischen 10-100 IU/ml sollte eine Auffrischung innerhalb eines Jahres mit anschließender Kontrolle erfolgen, bei anti-HBs <10 IU/ml sollte sofort nachgeimpft werden.
Dr. med. Frank Tacke
Medizinische Klinik III, Universitätsklinikum Aachen
Pauwelsstr. 30, 52074 Aachen
Tel. 0241-8035848, Fax 0241-8082455
Email: frank.tacke@gmx.net
Literatur
1. Deutsche Gesellschaft für Verdauungs- und Stoffwechselerkrankungen. Leitlinien Hepatitis B Virusinfektion. Z Gastroenterol 2004; 42: 677-702
2. Trautwein C, Tacke F. Therapie der Hepatitis-B- und -C-Virusinfektion. Dtsch Med Wochenschr 2003; 128(Suppl 2):87-89
3. Poland GA, Jacobsen RM. Prevention of hepatitis B with the hepatitis B vaccine. New Engl J Med 2004; 351(27):2832-2838
4. Tacke F, Amini-Bavil-Olyaee S, Heim A, Luedde T, Manns MP, Trautwein C. Acute hepatitis B virus infection by genotype F despite successful vaccination in an immune-competent German patient. J Clin Virol 2007; 38(4):353-357
5. Schaefer S. Hepatitis B virus taxonomy and hepatitis B virus genotypes. World J Gastroenterol 2007; 13(1):14-21
6. Tacke F, Manns MP, Trautwein C. Influence of mutations in the Hepatitis B Virus genome on virus replication and drug resistance - implications for novel antiviral strategies. Curr Med Chem 2004; 11(20):2667-2777
7. Harford N, Cabezon T, Colau B, Delisse AM, Rutgers T, De Wilde M. Construction and characterization of a Saccharomyces cerevisiae strain (RIT4376) expressing hepatitis B surface antigen. Postgrad.Med.J. 1987; 63 (Suppl 2):65-70.
8. Seddigh-Tonekaboni S, Waters JA, Jeffers S, Gehrke R, Ofenloch B, Horsch A, Hess G, Thomas HC, Karayiannis P. (2000) Effect of variation in the common "a" determinant on the antigenicity of hepatitis B surface antigen. J Med Virol 2000; 60:113-121





