DR. ROLF KAISER, KÖLN
HBV-Resistenztest
In den neuen Leitlinien zur Diagnostik und Therapie der chronischen Hepatitis B spielen virologische Aspekte eine wichtige Rolle. Für Auswahl und Monitoring einer Therapie sind die Bestimmung der HBV-Viruslast, des HBV-Genotyps und die Analyse von Resistenzen gegenüber den verschiedenen Polymerase-Inhibitoren sinnvoll. Dazu stehen molekularbiologische Analysen sowie frei verfügbare Interpretationssysteme für die Vorhersage von HBV-Genotyp, Vaccine-Escape-Mutanten und Resistenzen gegenüber Nukleos(t)id Analoga zur Verfügung.
Das Phänomen der Resistenzentwicklung ist aus der Therapie bakterieller Infektionen mit Antibiotika und aus der Therapie der HIV-Infektion mit antiretroviralen Medikamenten bekannt. Sollte die HBV-Viruslast sechs Monate nach Beginn der antiviralen Therapie noch nicht unter der Nachweisgrenze liegen bzw. nicht weiter abfallen, besteht die Möglichkeit einer Resistenz. Man sollte den neuen Leitlinien zufolge dann die Therapie intensivieren. Um dabei das weitere Vorgehen möglichst rational zu gestalten, ist ein Resistenztest sinnvoll.
RESISTENZ-MUTATIONEN
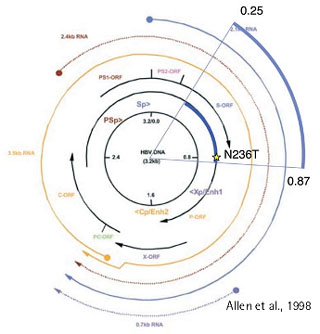
Abb. 1: Schematische Darstellung des HBV- Genoms. Mit der PCR in dem gezeigten Bereich lässt sich eine Region im HBV amplifizieren, die gleichzeitig Auskunft gibt über das HBs-Antigen und die HBV-Polymerase. Damit kann sowohl HBV-Genotyp (A-F), eine mögliche Vaccine-Escape Mutante (am häufigsten G145R) und Resistenz gegenüber den antiviralen Medikamenten erkannt werden.
Ähnlich wie bei HIV steht mittlerweile auch für HBV die Möglichkeit der Resistenz- testung mittels Sequenzanalyse zur Verfügung (genotypische Resistenztestung). Bei HBV ist das Surfacegen und das Polymerasegen in derselben Region des Genoms in unterschiedlichen Leserastern codiert. Deshalb können bei einer Sequenzanalyse gleich zwei Gene analysiert werden. Mehrere Publikationen zeigen, dass ein Therapieversagen unter Lamivudin (3TC) mit einer entsprechenden Resistenzentwicklung gekoppelt sein kann. Die Mutationen V173L, L180M und M204I/V bzw. Kombinationen derselben (früher YMDD-Mutation genannt) führen zu einer vollständigen Unwirksamkeit von 3TC2. Für die Resistenz von HBV gegenüber Adefovir (ADF) sind bislang drei Mutationen - A181V, N236T und I233V - beschrieben worden3, 4. Gegenüber Entecavir (ETV) besteht eine Resistenz, wenn mindestens eine der Mutationen T184A/G/I/S, S202G/I und M250V in Verbindung mit den Mutationen L180M und M204I/V vorliegt5. Eine genotypische Resistenzbestimmung der entsprechen Region von HBV gibt zudem Aufschluss über das Vorhandensein von Vaccine-Escape-Mutanten, die resistent sind gegenüber der passiven und aktiven Immunisierung. Die häufigste Mutation hier ist die G145R im Surfacegen (HBs-Ag)6.
WANN RESISTENZTEST?
Zusammenfassend gibt es drei Gründe für die molekularbiologische Analyse von HBV:
- Zur Bestimmung des Genotyps als Entscheidungshilfe bei der Therapiewahl;
- Zur Beantwortung der Frage, ob eine aktive oder passive Immunisierung möglich ist;
- Zur Bestimmung der Resistenz gegenüber antiviralen Medikamenten, also bei virologischem Versagen, bei Verdacht auf Übertragung eines resistenten HBV, vor einer möglichen Intensivierung einer Therapie durch ein weiteres Medikament.
VORGEHEN IN DER PRAXIS
Abb. 2: Die Startseite des frei im Internet verfügbaren HBV-Interpretationssystems, das unter www.genafor.org zu erreichen ist.
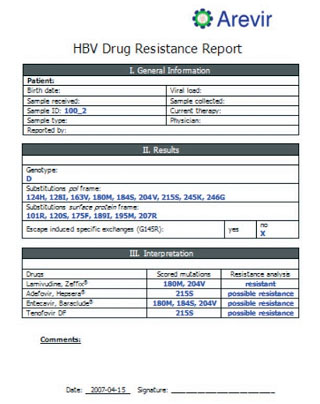
Abb. 3: Report des Interpretationssystems. Bei diesem Virus handelt es sich um ein HBV Genotyp D. Damit liegt ein für die Interferon- therapie ungünstiger Genotyp vor. Die häufigste der Vaccine-Escape Mutationen, die G145R liegt nicht vor. Es besteht Resistenz gegenüber 3TC (Lamivudin, Zeffix), die Sensitivität gegenüber ETV (Entecavir, Baraclude) ist herabgesetzt, ein klinischer Erfolg ungewiss. Die Sensitivität gegen- über ADF (Adefovir, Hepsera) und TDF (Tenofovir, Viread) ist wahrscheinlich reduziert, klinisch aber wahrscheinlich noch wirksam. Aufgrund der Therapiehistorie, in der der Patient bereits 3TC bzw. ADF bekommen hatte, wurde bei dem Patienten jetzt eine Therapie mit TDF eingeleitet. Kombinationstherapien standen auf- grund der vorhandenen Kreuzresistenzen nicht zur Debatte. Die Therapie mit TDF führte jedoch zu einer Viruslastabsenkung unter die Nachweis- grenze (6 IU/ml).

Abb. 4: Interpretation des ebenfalls frei im Internet verfügbaren HBV-Tools, das über www.hiv-grade.de zu erreichen ist. Es han- delt sich hier um HBV mit Genotyp F, ohne bekannte Vaccine-Escape Mutationen (hier nicht gezeigt). Es besteht Resistenz gegen- über 3TC. Die Suszeptibilität gegenüber ETV wird als eingeschränkt beurteilt. Als Option für diesen Patienten kommen ADF und TDF in Betracht, bei ETV besteht die Möglich- keit einer höheren Dosierung, da bereits eine reduzierte Empfindlichkeit vorliegt.
Welches Material wird benötigt? Die molekularbiologische Analyse erfordert EDTA-Blut, das ungekühlt transportiert werden kann. Einfrieren des EDTA-Bluts oder Lagerungen bei -20°C sind nicht vorteilhaft und beeinflussen die Nachweisegrenze ungünstig. Die HBV-Viruslast (HBV-DNA) und die Genotyp/Resistenzbestimmung kann aus derselben Probe analysiert werden. Normalerweise sind 5 ml EDTA Blut für die beiden Teste ausreichend. Für die Bearbeitung der Probe sollten etwa zwei Wochen eingeplant werden.
METHODEN
Zur Durchführung stehen ein kommerzielles System (Siemens-Trugene) und verschiedene in-house Systeme zur Verfügung. Die erhaltenen Analysen aus allen bekannten Systemen können über frei im Internet verfügbare Programme interpretiert werden, z.B. www.genafor.org und www.hiv-grade.de.
Beide Systeme machen gleichzeitig Vorhersagen über HBV-Genotyp, Vaccine-Escape-Mutante und Resistenz gegenüber Nukleos(t)id Analoga, da in einer Region zwei Gene (Surface- und Polymerasegen) codiert werden. Phänotypische Resistenzteste sind derzeit noch so aufwändig, dass sie routinemäßig nicht zur Verfügung stehen.
VIROLOGISCHE LABORE
Durchgeführt wird die Genotyp-Bestimmung/Resistenztestung in verschiedenen Universitäten, z.B. den Instituten für Virologie der Universitäten München, Düsseldorf, Bonn, Frankfurt und Köln sowie dem Institut für Pathologie der Universität Tübingen. Anfragen können auch an Labore im niedergelassenen Bereich gerichtet werden, z.B. an das Labor Berg, Berlin, an das Institut für Immunologie und Genetik, Kaiserslautern und an die Synlab-Gruppe. Diese Liste hat keinen Anspruch auf Vollständigkeit, daher sollte zunächst beim eigenen Labor nachgefragt werden.
ERSTATTUNGSFÄHIGKEIT
Zur Abrechnung ist festzustellen, dass es sich um einen Test handelt, der noch nicht im EBM-Katalog aufgelistet ist, obwohl der Nutzen eindeutig erwiesen ist. Für die Kostenübernahme muss bei ambulanten Patienten, die nicht privat versichert sind, ein Einzelantrag geschrieben werden, um eine taugliche Therapie auszuwählen und somit untaugliche und damit unnötige Kosten verursachende Therapien zu vermeiden. Eine untaugliche Therapie führt zu einer erniedrigten Lebenserwartung des Patienten und ist mit erheblichen Kosten verbunden, die durch stationäre Aufenthalte oder andere kostenintensive Maßnahmen verursacht werden. Sehr häufig besteht klinisch der Verdacht auf Resistenz gegenüber 3TC, der sich im Resistenztest nicht bestätigt.
Die Kosten für eine molekularbiologische Untersuchung auf HBV-Genotyp, Vaccine Escape und Resistenz gegenüber den derzeit verfügbaren anti-HBV Medikamenten betragen € 439,29 (entspr. GOÄ 4780, 4784, 4786, 2X4787).
Maßgeblich beteiligt an den Projekten sind Martin Däumer, Ulrike Schuldenzucker, Joachim Büch, Thomas Lengauer, Martin Obermeier, Dörte Hammerschmidt, Nadine Sichtig. Dr. Rolf Kaiser · Institut für Virologie der Universität zu Köln · Fürst Pückler Str. 56 · 50935 Köln · Email: rolf.kaiser@uk-koeln.de
Literatur
1. Janssen HLA et al. (2005) "Pegylated Interferon alpha-2b alone or in combination with 3 TC for HBe-Antigen positive chronic Hepatitis B patients: a randomised trial " Lancet 365, 123 - 129.
2. Pillay D et al. (1998) "Mutations in the hepatitis B virus DNA polymerase associated with antiviral resistance." International Antiviral News 6/9 167 -169.
3. Villeneuve JP, Durantel D, Durantel S, Westland C, Xiong S, Brosgart CL, Gibbs CS, Parvaz P, Werle B, Trepo C, Zoulim F. (2003) "Selection of a hepatitis B virus strain resistant to adefovir in a liver transplantation patient." J Hepatol. 2003 Dec;39(6):1085-9.
4. Schildgen O, Sirma H, Funk A, Olotu C, Wend UC, Hartmann H, Helm M, Rockstroh JK, Willems WR, Will H, Gerlich WH. (2006). "Variant of Hepatitis B Virus with Primary Resistance to Adefovir." NEJM 354: 1807-1812.
5. Shaw T., Bartholomeusz A., Locarnini S. (2006) HBV drug resistance: mechanisms, detection and interpretation. J Hepatology, 44: 593-606.
6. Carman WF et al. (1990) "Vaccine-induced escape mutant of Hepatitis B virus." Lancet 336:325-329.





